上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
公司新闻/正文
七种外泌体示踪技术,让外泌体无所遁形!
2800 人阅读发布时间:2020-11-18 13:09
外泌体作为细胞间通信的短距离和长距离纳米载体,具有许多生物学功能。它们允许细胞之间复杂信息的交换,从而在生理和病理条件下调节各种过程,例如体内稳态、免疫反应和血管生成。此外,由于它们具有独特的迁移、靶向和选择性内化进入特定细胞的能力,是非常有前途的传递载体。
外泌体的这些特性,为诊断和治疗提供了潜在的新领域,并可替代基于细胞的治疗方法。然而,将外泌体治疗转诊至临床的主要缺点是目前对这些内源性囊泡的了解还不足,尤其是在体内行为方面。
体内追踪外泌体可以提供有关其生物分布、迁移能力、毒性、生物学的重要知识角色,沟通能力和行动机制。今天小编将介绍不同的外泌体标记和成像方法,从而可以对其体内的生物分布、生理功能、迁移和靶向机制进行体内研究。
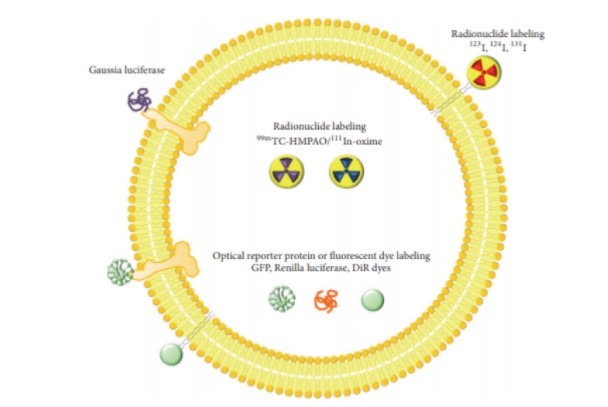
Figure: Strategy for labeling of extracellular vesicles.GFP;green fluorescent protein,DiR; near infrared fluorescent dye.
1. 磁成像(magnetic imaging)
示踪外泌体
MRI(magnetic resonance imaging)具有诸如无辐射和高空间分辨率的优点。为了能够通过MRI进行检测,必须用磁性造影剂,比如超顺磁性氧化铁纳米颗粒SPIONs标记外泌体。
MRI可以进行纵向成像-研究结果显示了静脉注射后长达12天的成像(Jc Bose等人,2018),可高分辨率并大程度地穿透深层结构。但必须考虑到,在整个持续时间内,纳米粒子可能不会全部包含在外泌体中,并且图像可能反映了SPIONs在外泌体融合后进入细胞,因此这种方式不一定能够提供有关外泌体最终命运的信息。
2. CT(computed tomography)
示踪外泌体
CT是广泛使用的具有高空间和时间分辨率的一种医学成像技术。其工作原理基于组织对X射线的吸收差异,形成由多个横截面图像组成的三维图像。
CT的一个重要优点是它可通过功能成像方法[例如正电子发射断层扫描(PET)和单光子发射计算机断层扫描(SPECT)]执行融合成像。与MRI一样,造影剂和纳米材料通常用于增强CT信号。
CT提供了广泛可用的成像方式,能够以优异的穿透力在整个身体中以良好的分辨率跟踪外泌体。但这种方式需要直接标记外泌体,并具有与该过程相关的所有缺点,例如无法确定图像中出现的信号是指实际的外泌体还是泄漏或转移的内容物,同时还存在与任何CT成像相关的电离辐射问题。
上图,文章“In Vivo Neuroimaging of Exosomes Using Gold Nanoparticles”基于葡萄糖涂层金纳米粒子(glucose-coated gold nanoparticle,GNP)标记,同时使用结合CT成像进行外泌体跟踪的方法。
文章直接用GNP标记外泌体,这与通过亲代细胞进行的典型且效率较低的间接标记方式相反。在机制水平上,作者发现葡萄糖涂层的GNPs是通过葡萄糖转运蛋白GLUT-1介导并涉及胞吞蛋白的活性,能量依赖性机制摄取到MSC衍生的外泌体中。接下来,文章证明了5 nm GNPs能够改善外泌体标记,并且与静脉内相比,鼻内给药可导致优异的大脑积聚,从而增强体内神经成像。
此外,文章使用局灶性脑缺血的小鼠模型,无创跟踪了鼻内给予GNP标记的外泌体,与非特异性迁移和同期对照脑的清除相比,其在病变部位的积累超过24小时。因此,这种外泌体标记技术可用作各种脑部疾病的强大诊断工具,并可能增强基于外泌体的神经元恢复治疗。
3. 核成像(nuclear imaging)
示踪外泌体
涉及在疾病的诊断和治疗中应用放射性物质的核成像被广泛用于细胞成像。放射性核素发出的辐射可以使用特殊的照相机在体内进行检测。由于放射性核素的半衰期很短,因此只会有相对短的成像和跟踪时间,但核成像可以通过提高灵敏度和组织穿透能力使深层结构和器官可视化。这种方法中,标记剂(比如Indium-oxine)通过孵育直接引入外泌体,通常使用单光子发射CT(SPECT)或正电子发射断层扫描(PET)获得3D图像,结合解剖学成像比如CT或MRI以提高其定位外泌体的能力。
4. 光声成像(Photoacoustic imaging)
示踪外泌体
光声成像(PAI)是最近开发的一种混合生物医学成像方法,它基于光声效应并将超声成像与光学成像相结合。
生物样品中的造影剂吸收脉冲激光辐射能量,并将其转换为声音信号,然后通过扫描换能器对其进行测量和可视化。因此,PAI是一种有吸引力的非侵入性成像方式,结合了高空间分辨率和超声成像深层穿透以及光学成像高对比度的优点。
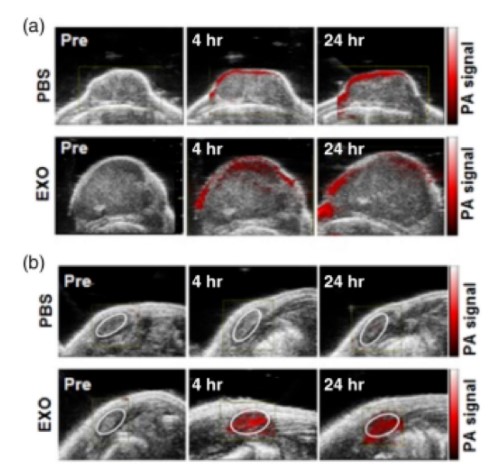
上图说明:静脉内(iv)注射三阴性乳腺癌模型中的癌细胞衍生外泌体后,对原发性肿瘤和腋窝淋巴结转移进行光声成像。(a)和(b)在肿瘤内注射抗EGFR-GN之前,4和24小时静脉注射磷酸盐缓冲液或外来体的小鼠的超声引导PAI。
5. 纳米颗粒(Nanoparticle)
分析示踪外泌体
纳米颗粒跟踪分析(NTA)基于以下原理:溶液中纳米颗粒的布朗运动速率与其大小有关。文章Plasma Exosomes Protect the Myocardium From Ischemia-Reperfusion Injury中将405 nm的激光(不同仪器可能有所不同)以固定的角度指向囊泡悬液,然后使用显微镜和高灵敏度相机捕获散射光。通过跟踪各个纳米粒子随时间的运动,软件可以计算其直径。NTA技术已被外泌体研究领域认可为外泌体表征手段之一,相较于其他表征方式,NTA技术的样本处理更简单、更能保证外泌体原始状态、检测速度更快,且能够测量多分散样品中的粒度分布。
6. 荧光成像(fluorescence imaging)
示踪外泌体
光学成像是分子和细胞生物学中流行的示踪技术,其中荧光显微镜是研究细胞和亚细胞代谢活性(特别是活细胞)的有力工具。荧光探针标记的分析物在激发时发出荧光信号,并由荧光显微镜记录信号。
荧光显微镜易于操作,能够实时且无创地追踪分析物,并且与多形式样品兼容。特别的是,荧光显微镜可以实时监测单个细胞的行为,这有利于观察外泌体与细胞之间的相互作用。迄今为止,有机染料、遗传编码的荧光蛋白、免疫荧光报告基因和荧光纳米材料已经用于标记外泌体。
1. 有机染料
亲脂性荧光膜染料将脂肪族的长尾巴插入外泌体的脂质双层中后发出强荧光信号。常用的报道分子包括PKH67(λex/λem= 490 / 502nm)、PKH26(λex/λem= 551/567 nm)、DiO(λex/λem= 484/501 nm)、DiI(λex/λem= 549/565 nm)、 DiR(λex/λem= 750/780 nm)和FM 4-64(558/734 nm)。这些有机染料都可以购买到,并在外泌体膜上发出稳定且持久的荧光信号,这有助于观察外泌体与受体细胞之间的相互作用,尤其是在体外。
有机染料的标记机理相同,但是在荧光量子化、颜色和半衰期等方面有所不同。有机染料的发射波长范围为502至734 nm,这为研究人员在选择合适的探针进行外泌体标记时提供了多种选择。在实践中,用亲脂性染料标记的外泌体脂质可能无法反映其确切的半衰期,因为有机染料还可以染色其他脂质实体并保留很长时间,从而提供错误的阳性信号并干扰外泌体命运的准确时空评估。另一方面,荧光化学标记方法仅适用于来自条件培养基或体液的纯化外泌体,但无法染色原始细胞中的外泌体,然后追踪其在细胞间的移动。
2.外泌体标志蛋白与荧光融合质粒/病毒
使用分子生物学方法将荧光蛋白(例如绿色荧光蛋白GFP;红色荧光蛋白RFP)与外泌体膜上的标记蛋白如CD63、CD9、CD81等融合表达可以跟踪外泌体从供体到受体细胞的运动。通过监测膜蛋白的荧光,可以实现活体培养物中和体内外泌体转移的直接可视化。此外,由于荧光蛋白特异性地缀合到外泌体上,因此这种标记策略避免了标记其他脂质实体的假阳性信号。文章常见的就是构建CD63(四跨膜蛋白家族中的一员,被认为是外泌体膜标记物)与荧光蛋白融合质粒或者病毒,可追踪外泌体在肿瘤,免疫系统和神经发生中的途径。
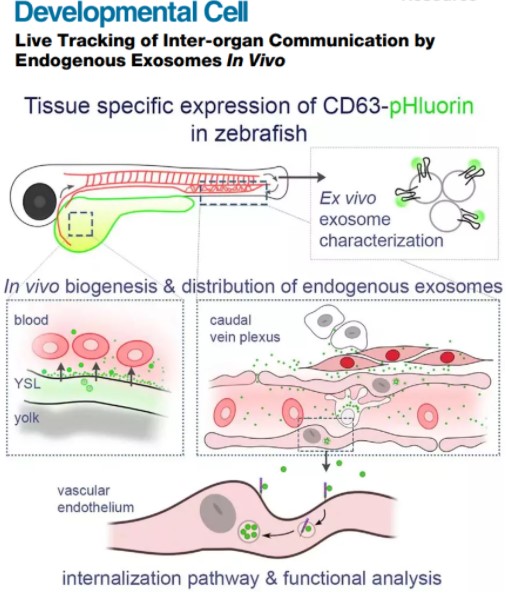
文章“Live Tracking of Inter-organ Communication by Endogenous Exosomes In Vivo” 开发了一种斑马鱼胚胎模型,通过在斑马鱼胚胎中表达CD63-pHluorin,使用成像方法和蛋白质组学分析的组合,研究内源外泌体的组成和控制其生物发生、命运和对靶细胞作用的分子机制。
研究人员在斑马鱼胚胎中表达CD63-pHluorin报告基因,用于示踪体内外泌体。该荧光报告分子特异性地靶向(晚期)内体并在外泌体上分泌,允许体外单个细胞中外泌体的释放可视化。结合成像方法和label-free蛋白质组学定量分析,从而实现在整个动物体内追踪直至到达最终目的地,并揭示其生物学功能。研究发现外泌体从卵黄合胞体层(YSL)大量释放到血流中,这些外泌体被尾静脉丛的巨噬细胞和内皮细胞捕获、内吞和降解,具有清除剂受体和活力依赖性。
总之,研究首次揭示了体内内源性外泌体的分泌、扩散和被靶细胞摄取以及这些过程的关键分子介质。
7. 生物发光成像(bioluminescence imaging)示踪外泌体
生物发光成像(BLI)使用自然生物过程产生的光(即荧光素酶-底物反应)和用于信号检测的超灵敏相机。常用的荧光素酶基因有萤火虫荧光素酶(Fluc)、高斯普林斯荧光素酶(Gluc)或海肾荧光素酶(Rluc)。
生物发光不需要激发源来发光,而是通过各自的底物与ATP和Mg2 +或单独的氧气反应来发出生物发光。生物发光成像(BLI)的高灵敏度和低背景信号质量使荧光素酶基因成为体内研究报告基因的好选择。下图是小鼠静脉注射GL标记的B16-BL6来源外泌体后,GLuc的动力学变化图。具体做法是:pCMV-gLuc-lactadherin质粒转染B16-BL6细胞后,收集的外泌体静脉注射Balb/c小鼠。然后同时静脉注射腔肠素后于10、30、60和240分钟对表达gLuc的 B16-BL6细胞来源外泌体进行成像。
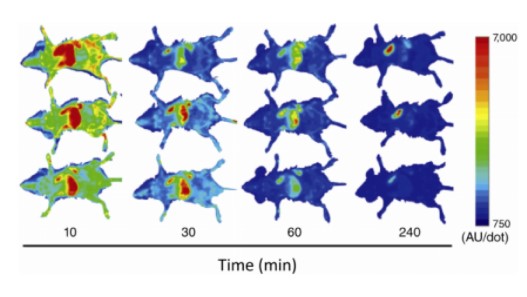
生物发光成像(BLI)技术提供了外泌体生物分布的全身图片,并且由于标记是固有的,因此外泌体跟踪非常可靠。生物发光成像(BLI)还提供了有关外泌体参与过程的数据,例如揭示了细胞通过外泌体影响其微环境的机制。但需要在每次成像之前注入底物,并且底物(例如腔肠素)的半衰期非常短,因此需要非常长时间、快速而准确的成像系统。此外,任何基于荧光的体内成像在分辨率和穿透深度上都受到限制,因此无法清晰显示外体在深层身体结构中的位置。
因此,该技术最适合临床前研究。与FLI相比,BLI具有极低的信噪比,这是因为哺乳动物组织中的自发光可忽略不计。
吉凯基因可以提供不同标记(生物发光和化学发光)的CD63现货慢病毒,可选有EGFP、Cherry、EYFP、Firefly_Luciferase等不同标记,同时我们可以根据您的要求进行个性化定制,比如CD9、CD81外泌体标志蛋白。另外,吉凯基因提供外泌体一站式解决方法,如果有老师想做外泌体,可以前来咨询,我们不仅给您提供有效的研究思路,更切实帮您解决实验中的具体问题。

赶快扫描来咨询吧↑
吉凯基因,年产上万次慢病毒、腺病毒、腺相关病毒;
建有国内大型的慢病毒文库,包含几乎覆盖人类所有基因的,近 15 万个独立克隆;
建有国内大型的慢病毒文库,包含几乎覆盖人类所有基因的,近 15 万个独立克隆;
国内集产品采购和资讯分享的一体化综合服务平台,为科研工作者提供一键式的采购服务,产品周期短至 5 个工作日起;
18 年品质保证、助力客户发表 10000+ 篇 SCI,多项科研成果发表于 Nature Medicine、Nature Immunology、Gastroenterology、Cell Metabolism、Nature Neuroscience 等著名期刊上