上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
公司新闻/正文
Neuron:杏仁核线粒体自噬的增加或是引起焦虑的关键机制!
5604 人阅读发布时间:2022-04-13 18:23
焦虑是对潜在或预期威胁的持续性恐惧,偶尔的焦虑是一种正常的情绪状态,但持续的、破坏性的或压倒性的焦虑就像焦虑症一样,会严重影响正常的工作和生活。长期的社会心理压力会引起焦虑,但其影响焦虑的细胞生物学机制尚不清楚[1]。
长期的压力对动物脑内线粒体有明显的影响。有研究发现啮齿动物的慢性轻度应激会导致大脑线粒体形态和呼吸活动的改变以及类似抑郁的行为,这说明大脑线粒体异常可能与行为失调之间存在联系。
在人类相关研究中也发现,精神疾病患者大脑中的线粒体形态、功能和蛋白的表达发生了改变。尽管线粒体、压力和行为之间存在着这些联系,但是线粒体紊乱是否是压力相关的行为改变的原因或结果还有待研究[2]。
2021年12月1日,来自美国国立心理卫生研究所的Zheng Li课题组在Neuron上发表了题为”Mitophagy in the basolateral amygdala mediates increased anxiety induced by aversive social experience”的工作,确定了线粒体吞噬在心理遗传应激引起的焦虑中的作用,并揭示了线粒体缺失增加焦虑的现象,并提出线粒体和线粒体吞噬可能是缓解焦虑的靶点[3]。

01 CSD会引起杏仁核线粒体的改变
为了测试心理压力对线粒体的影响,研究者们采取了慢性社交挫败(chronic social defect,CSD)的范式。由于杏仁核是对恐惧和威胁经历的编码和处理中心,而腹侧海马参与压力反应和情绪反应,所以研究者们通过mito-YFP小鼠(特异性标记线粒体)观察了CSD处理30天后杏仁核和腹侧海马线粒体的变化。结果发现CSD组小鼠基底外侧杏仁核(basolateral amygdala, BLA)和杏仁核中央核(central nucleus of the amygdala, CeA)中线粒体的大小和总量都减少了。
但战败小鼠海马区中,只在齿状回(dentate gyrus, DG)观察到了线粒体变小的现象,并且CA1、CA3和DG区线粒体总量都没有发生变化(图1)。另外,CSD组小鼠BLA和CeA线粒体膜电位显著降低,但CA1、CA3和DG区的线粒体膜电位并没有明显改变,这说明30天CSD导致会影响BLA和CeA的线粒体膜电位去极化,但对腹侧海马影响不大。这些实验结果显示,30天CSD小鼠杏仁核线粒体多个方面都发生了改变(图2)。
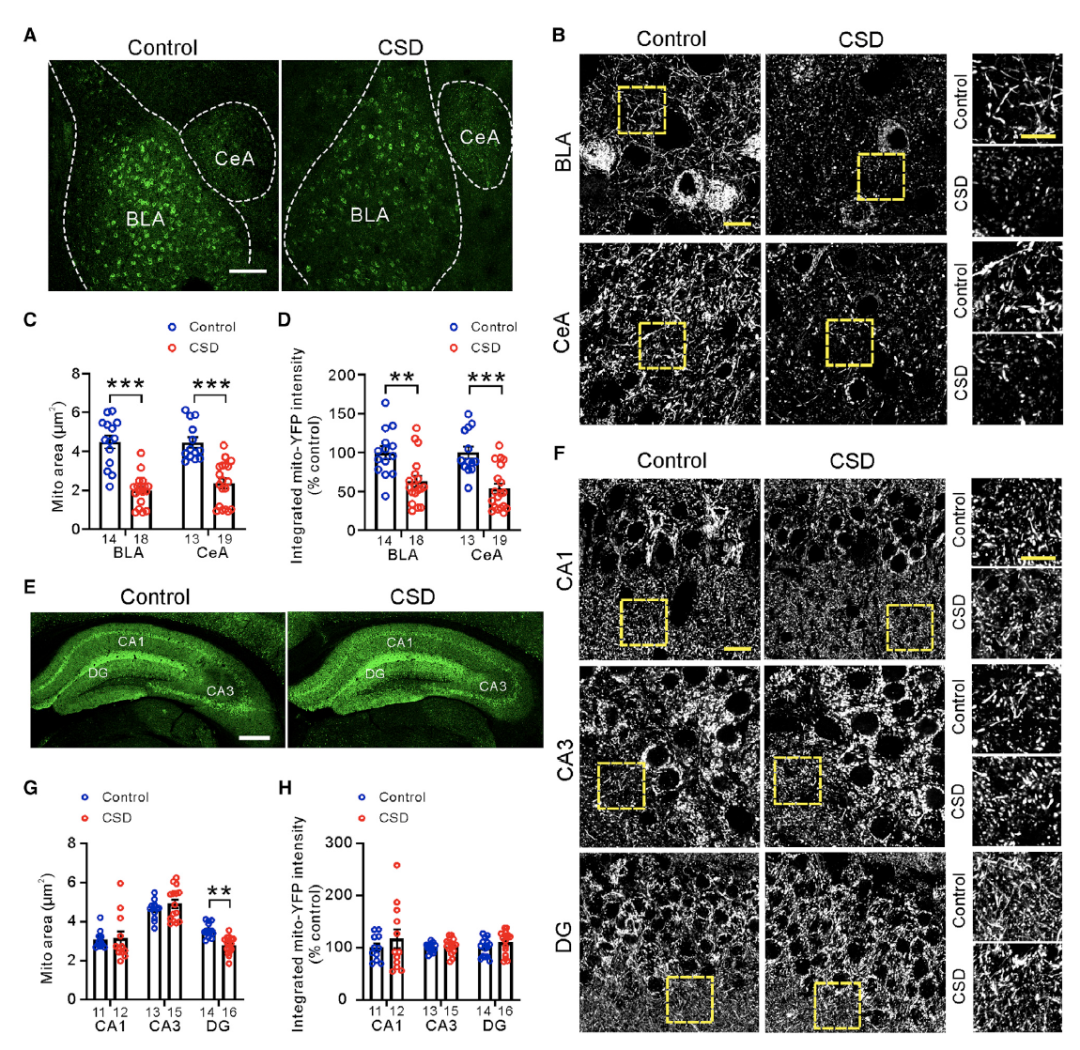
图1: CSD小鼠杏仁核线粒体数量减少、形状变小
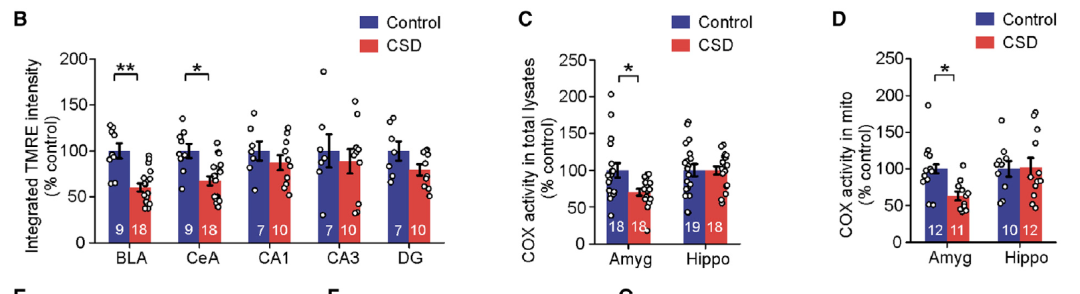
图2:CSD小鼠BLA和CeA线粒体膜电位显著降低
02 CSD小鼠杏仁核线粒体DNA复制增多,突变也增多
由于在30天CSD组小鼠杏仁核中观察到了线粒体丢失的现象,于是研究者们推测线粒体的新生和消除之间可能存在失衡。由于产生新的线粒体时会有线粒体DNA(mitochondrial DNA, mtDNA)的复制,于是研究者们通过EdU来标记新复制的mtDNA。结果显示被打败的CSD小鼠BLA中EdU阳性的线粒体数量增加,但在DG中没有观察到EdU的增加。mitoRCA-seq的数据显示,30天CSD小鼠杏仁核中all突变和transition突变的频率增加,但transversion突变的频率不变,这说明mtDNA复制可能导致mtDNA突变增加(图3)。
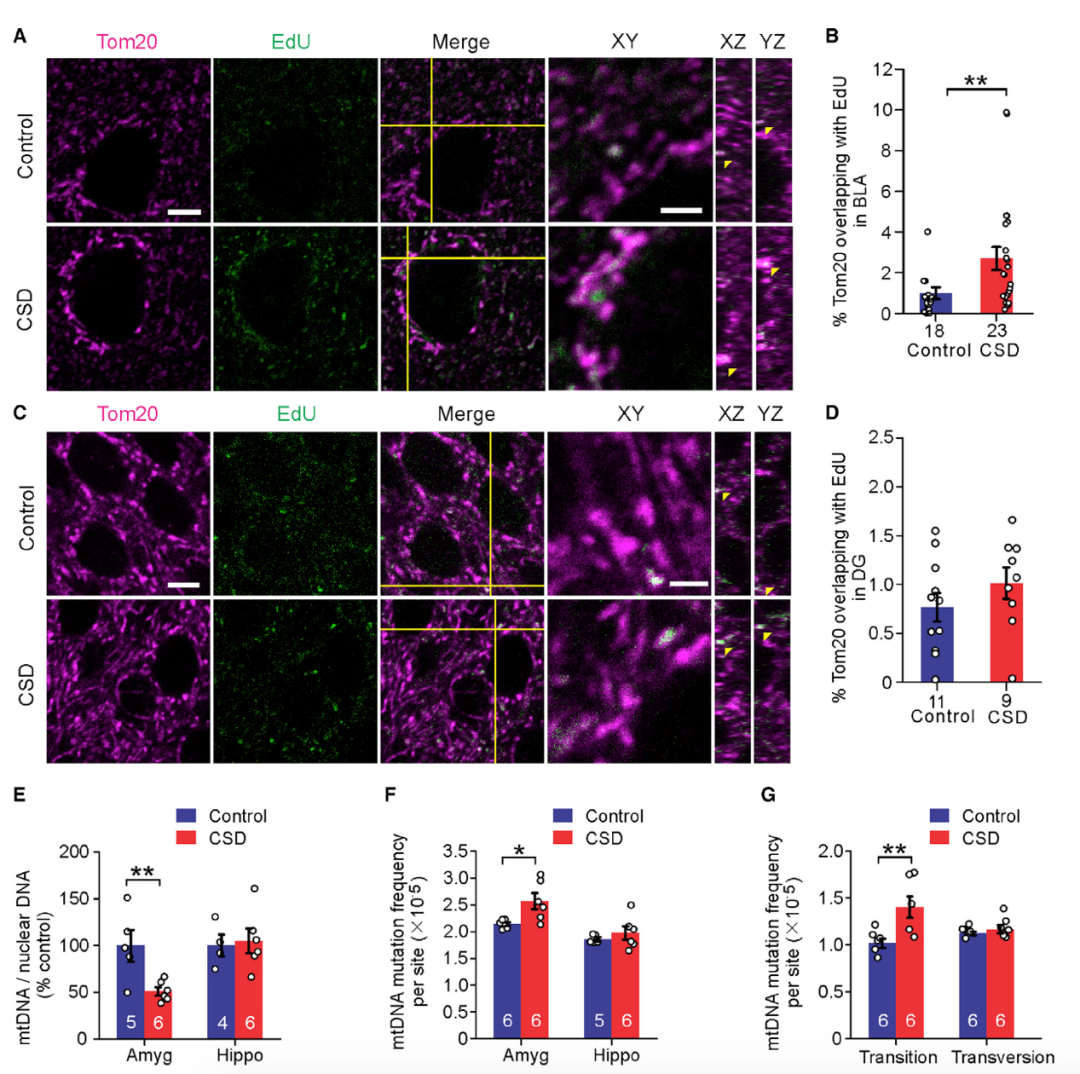
图3:CSD组小鼠BLA区线粒体新生增多,突变增加
03 CSD引起杏仁核线粒体自噬增加
接下来研究者们又对线粒体消失的过程—线粒体吞噬进行了研究。研究者们通过自噬体标记物LC3或optineurin来标记线粒体的自噬。结果显示,在30天CSD小鼠的BLA中,Tom20与LC3或optineurin的共定位显著增加。另外研究者们也将特异性靶向线粒体的KeimaRed (mitochondria-targeted, mtKeima)注射到小鼠的BLA脑区,并在CSD30天后观察溶酶体中mtKeima的含量,结果显示溶酶体中mtKeima也显著增多(图4)。这些结果表明30天的CSD处理使BLA中线粒体自噬增多。
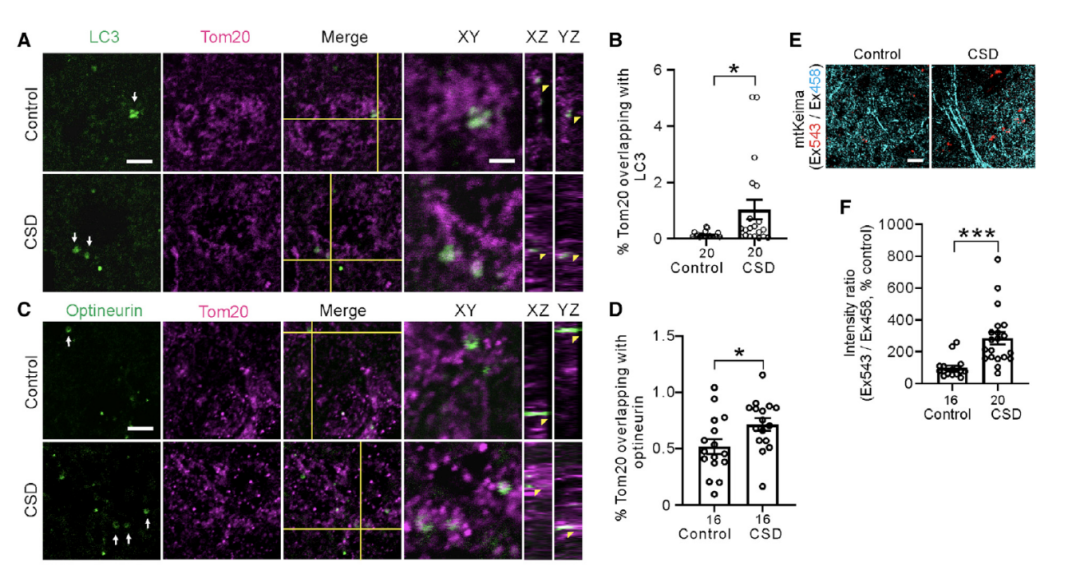
图4: CSD组线粒体自噬增多,且溶酶体中mtKeima增多
04 PINK1和Parkin介导CSD引起的线粒体自噬增加和线粒体丢失
之前有许多研究表明,PINK1和Parkin介导线粒体吞噬的过程。为了探究他们在CSD诱导的线粒体自噬增多中的作用,研究者们分别对Pink1-/-和Park2-/-进行了30天CSD造模。结果显示CSD组的Pink1-/-和Park2-/-小鼠BLA脑区的线粒体总量显著增多,但Tom 20和LC3的共定位并没有变化,这说明线粒体自噬没有被影响。这说明PINK1和Parkin参与了CSD引起的线粒体自噬增加的过程(图5)。
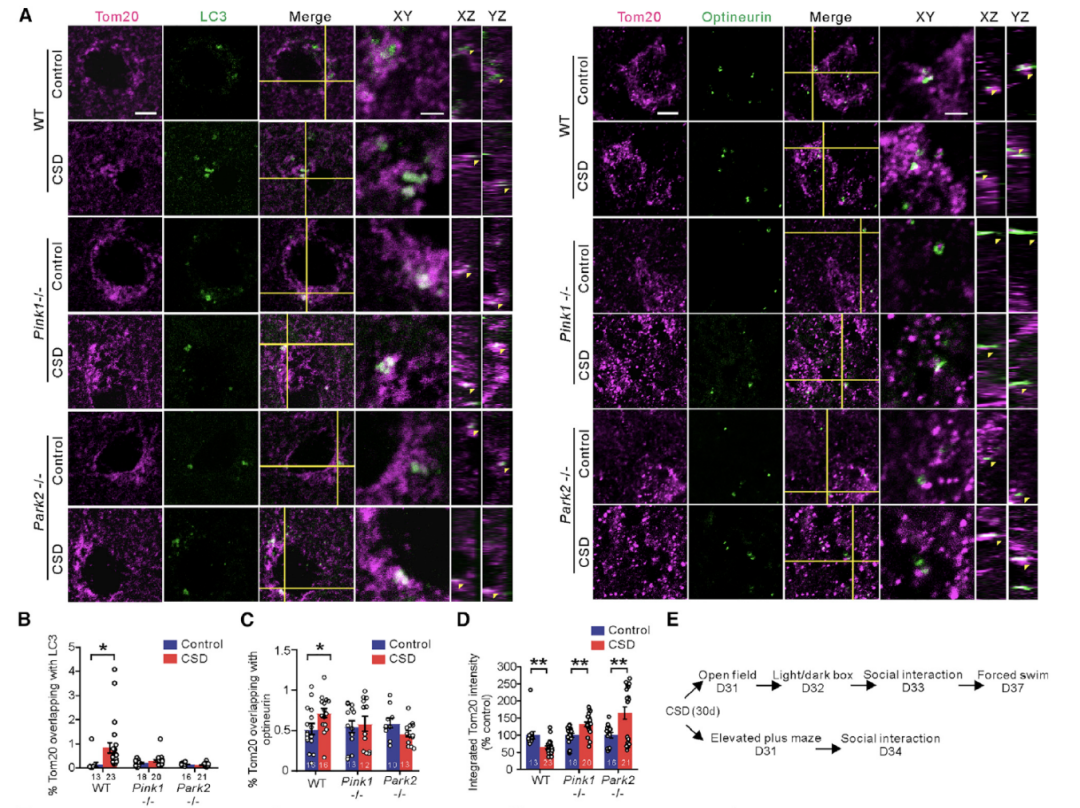
图5:PINK1和Pank2参与CSD引起的线粒体自噬过程
05 杏仁核线粒体缺失会引起焦虑样行为
为了测试杏仁核中线粒体缺乏是否会引起焦虑,研究者们向BLA区分别注射了靶向线粒体的KillerRed AAV(mitochondria-targeted KillerRed,mtKillerRed,一种荧光蛋白,在光照下会产生活性氧,破坏线粒体但不导致细胞死亡)和mtKeima AAV。结果显示,在脉冲光刺激后,注射mtKillerRed AAV组的小鼠抑郁样行为增加,但注射mtKeima AAV的对照组小鼠并无影响(图6)。
电镜的结果显示,脉冲光处理后mtKIllerRed组小鼠的线粒体样结构和异常线粒体的数量增加,线粒体数量减少,但自噬小体并未受影响。这些结果说明BLA线粒体缺失会增加焦虑样行为(图6)。
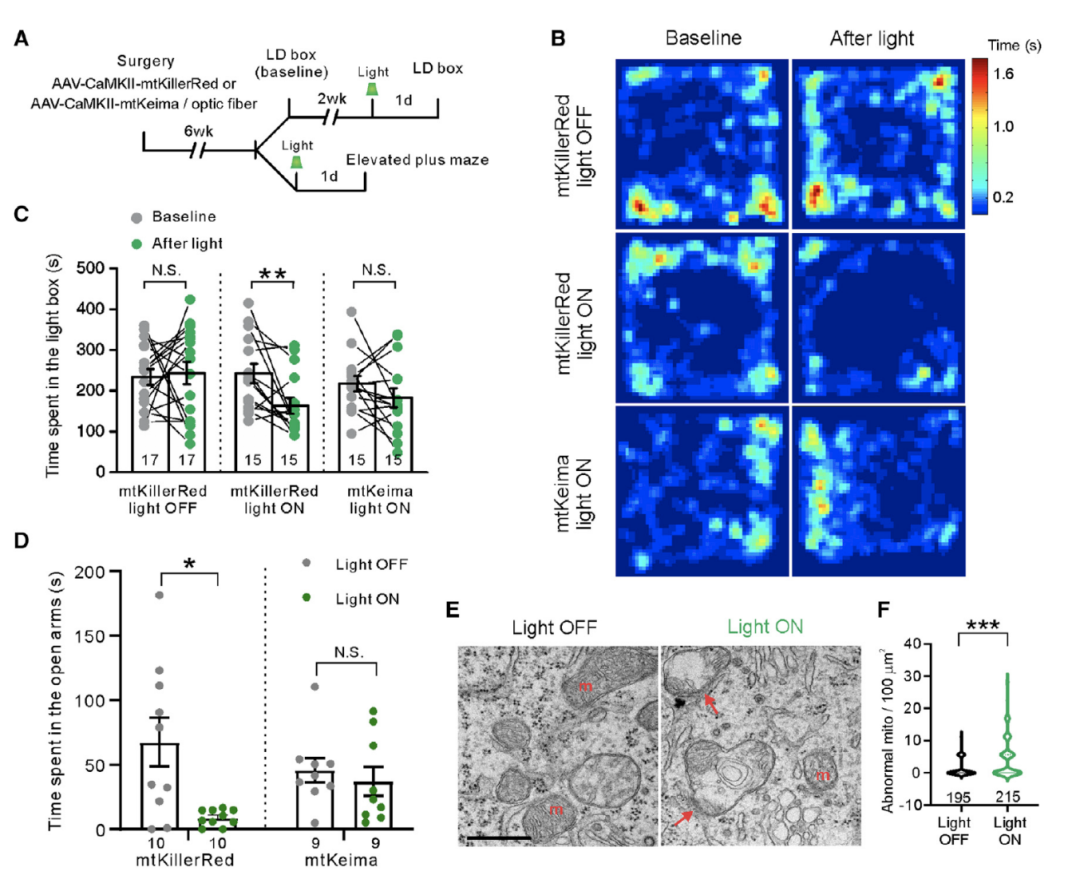
图6:人工诱导BLA区线粒体死亡会引起小鼠焦虑样行为
06 CSD小鼠BLA-BNST突触传递减弱
由于线粒体对突触的功能非常重要,因此研究者们对与焦虑相关的BLA-BNST通路中的突触传递进行了研究。于是他们在CSD前4周将表达channelrhodopsin 2 (E123A) 和 EYFP fusion proteins(ChR2-EYFP)的AAV注射到了BLA区,并在CSD后进行电生理的观察。结果显示,通过光遗传学的方法诱导神经元电活动后,CSD组小鼠的输入输出关系曲线向下偏移(图7A),这说明BLA-BNST的突触传递减弱了。
由于PINK1在CSD诱导的焦虑中起着非常重要的作用,研究者们进一步测试了PINK1对CSD突触效应的影响。于是他们向BLA中注射了ChR2 AAV的同时也注射了PINK1 siRNA病毒或者对照病毒,在CSD后对其电生理特性进行观察。结果发现在WT小鼠和注射了对照病毒小鼠中,CSD组I/O曲线下降,PPR升高,但PINK1 siRNA组小鼠中这些影响被消除了(图7)。
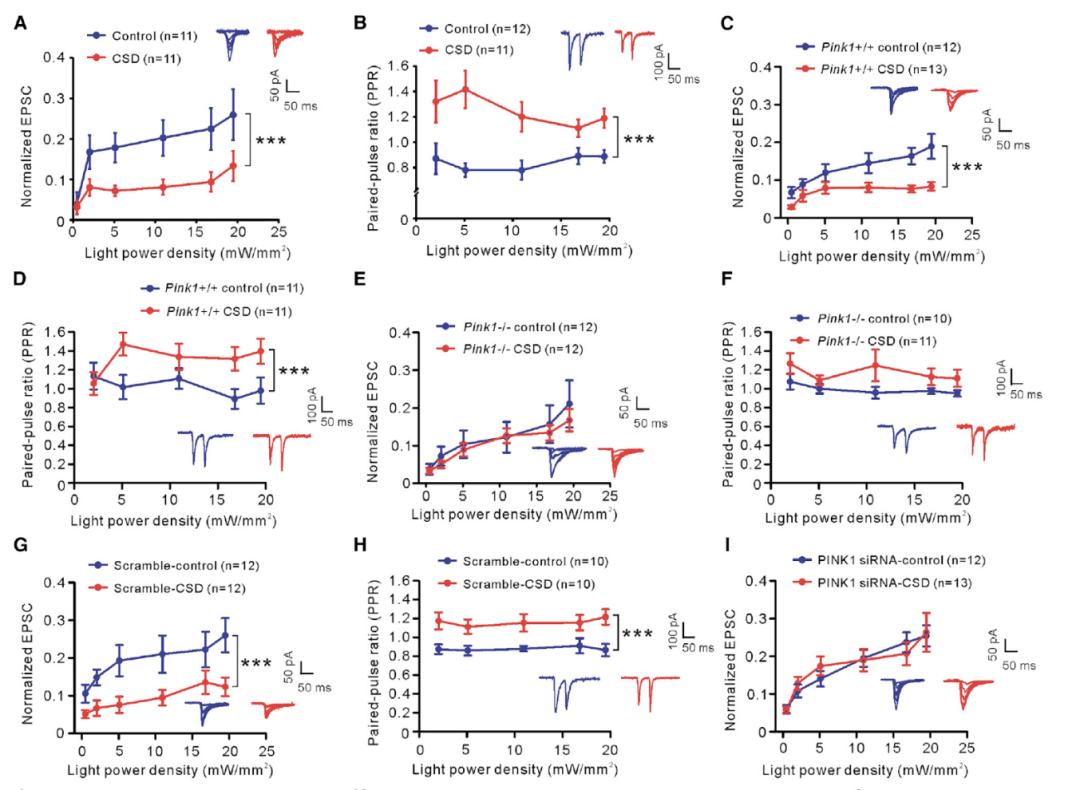
图7:CSD组小鼠BLA-adBNST突触联系减弱,敲除PINK1可以消除
为了进一步测试BLA-adBNST突触联系的减弱是否有助于CSD引起的焦虑效应,研究者们用光遗传的方法刺激CSD小鼠BLA到adBNST的投射。他们将ChR2 AAV注射到WT小鼠的BLA区,并在adBNST处植入了光纤。结果发现光照刺激在不影响运动的前提下,改善了小鼠的焦虑样行为(图8)。这些结果说明BLA-adBNST突触联系的减弱有助于增加焦虑样行为。
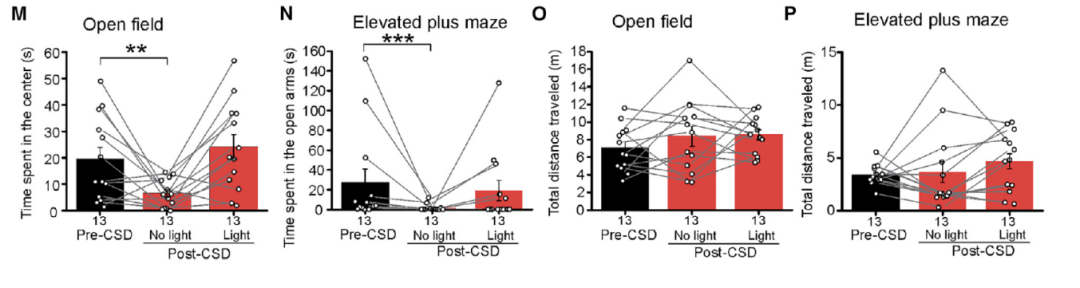
图8:BLA-adBNST突触联系减弱会引起小鼠焦虑行为
07 CSD小鼠杏仁核线粒体自噬增加与神经元激活相关
由于杏仁核参与情绪处理和社交行为,研究者们推测杏仁核强烈的神经活动可能会引起线粒体自噬,于是他们通过化学遗传学的方式进行了验证。他们将CaMKII启动子驱动的表达hM4Di的AAV注射到BLA区来抑制兴奋性神经元的电活动。结果发现CNO处理后BLA区LC3阳性的线粒体数量减少,并且CNO处理改善了CSD引起的社交回避和焦虑样行为(图9)。这说明CSD通过BLA区的神经活动增强引起线粒体自噬增加并引起焦虑样行为。
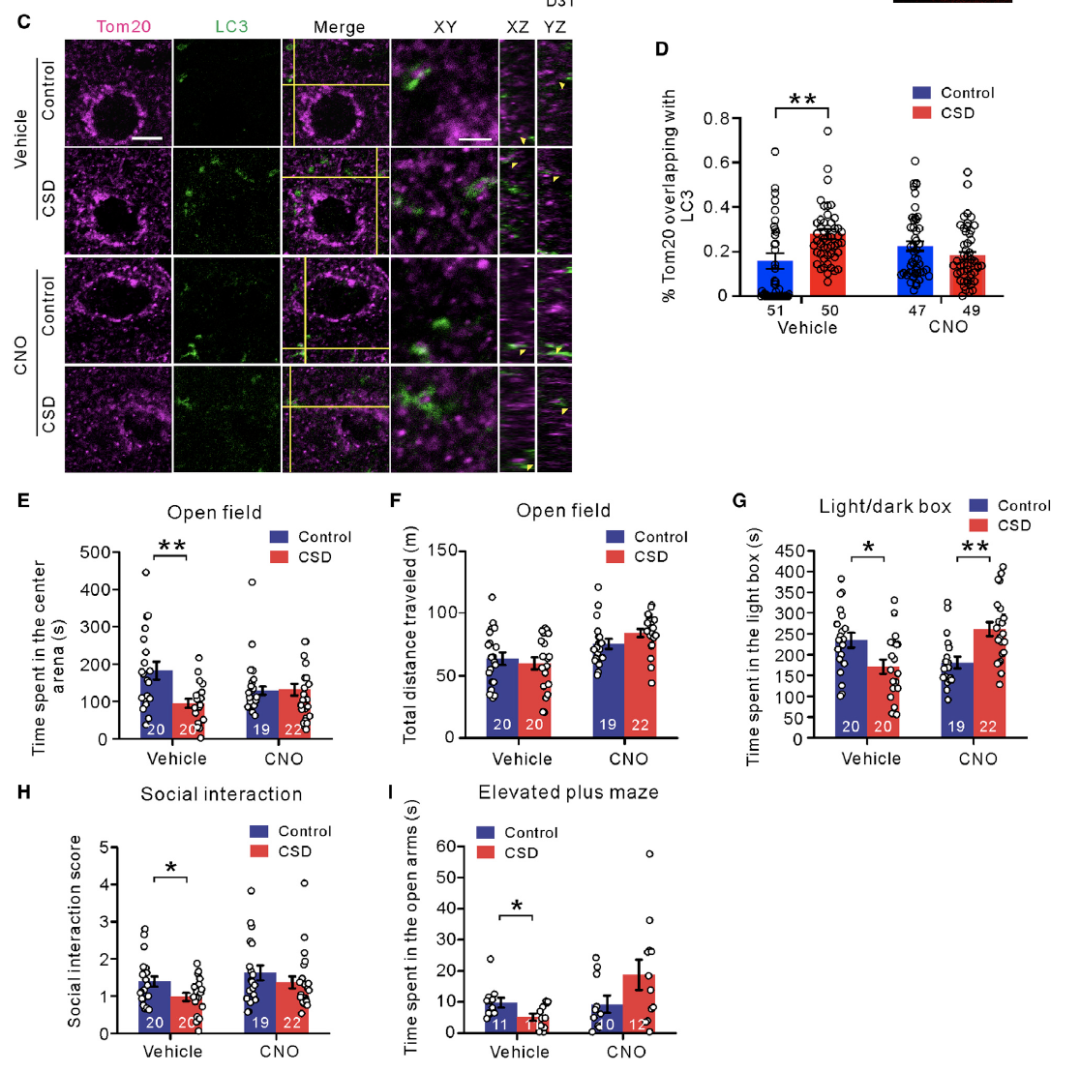
图9: CSD组小鼠BLA区的神经活动增强引起线粒体自噬和焦虑样行为
研究揭示了线粒体自噬在慢性心理应激过程中引起焦虑的关键性作用。慢性应激引起线粒体自噬增加,从而导致线粒体丢失,进而影响焦虑反应神经环路(BLA-BNST)的突触传递。因此,线粒体和线粒体自噬可能是改善焦虑的潜在靶点。