上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
空间代谢组学
询价
公司新闻/正文
一节课学会带肿瘤免疫抑制热点的国自然课题设计
1558 人阅读发布时间:2020-05-26 10:44
疫情期间,工作生活有种种不便,但是也抵挡不了广大科研工作者对科研的热情,正好也是趁着这个时间多学习多交流,毕竟国自然还有一个月就要交标书了。。。写好标书的老师要在这一个月再仔细修改,找专家帮忙评估,还没写好标书的老师那可要抓紧啦。
心系各位老师的吉凯基因也没闲着,我们除了安排一批专业博士进行公益标书评估活动,还安排了一系列围绕国自然课题设计、前沿技术的直播讲座,场场爆满,人气过万。最近的一场是关于临床科研课题设计思路之肿瘤免疫抑制的,获得听众们的好评和高度认可,那么下面我们就来简单回顾一下这不到一小时的一节课是怎么介绍国自然课题设计的,还能搭上肿瘤免疫抑制的热点顺风车。
第一部分 临床科研课题设计思路
经过吉凯基因一帮博士们几年的积累,我们总结出一个临床科研课题的研究模式,就是:A 基因通过调控 B 信号通路影响 C 疾病的 D 功能。这个模式对于做科研的老师来说肯定是不陌生的,这个模式下,课题的研究内容主要包括筛选具有临床相关性的 A 基因,A 基因的功能,以及 A 基因的作用机制。与临床相关的 A 基因包括与疾病发生发展相关的基因表达异常,或者突变、或者修饰异常等,所以我们可以从基因组、基因组表观遗传、转录组、蛋白质组层面,从与临床问题相关的组织样本中筛选 A 基因。紧接的第二块内容要研究 A 基因的功能,根据临床问题选择合适的细胞模型和动物模型,进行功能研究。找到 A 基因,也确认 A 基因有功能了,下面就是要进行机制研究了,机制研究也是体现整个课题深度的部分,所以在一个课题中的占比是非常大的,所以下面就来重点介绍下机制研究思路。
从机制研究的深度上来说,机制研究模式分为三大类:第一类分子相关性研究,也即 A 基因改变后,导致下游 B 机制的改变,可以是 B 的表达改变、修饰改变,也可以是空间定位改变。要找下游 B,可以通过查文献,广撒网,找明星通路做验证,这种方式简单,但是可能需要多次尝试,而且创新性也不高。而随着对研究不断深入的需求,通过组学的技术比如测序、蛋白质组等技术方法分析 A 基因的下游分子,通过生信分析来解决机制的方向性问题,成为了很多高分文章采用的方法。找到改变的下游,那么 A 真的是通过 B 来行使功能嘛?
为了解答这个问题,就要进行第二类机制研究,功能相关性分析,主要采用的手段就是功能回复实验。举个例子,A 基因下调,细胞表现出功能改变,而且 A 下调使 B 基因表达也下调,那么把 A 基因下调的同时,把 B 基因上调,通过功能学检测功能是否被回复,若功能回复了,说明 A 下调的确是通过 B 行使细胞功能调控作用的。
第三类机制研究是直接互作,直接互作包括蛋白与蛋白、蛋白与 RNA、蛋白与 DNA、RNA 与 RNA 等,根据 A 基因本身的性质,选择合适的实验方法来进行分析验证,常用的实验方法包括 co-IP,Pull down,RNA-pull down,RIP,ChIP 等。
简单归纳一下一个临床科研课题的思路,如下图:
心系各位老师的吉凯基因也没闲着,我们除了安排一批专业博士进行公益标书评估活动,还安排了一系列围绕国自然课题设计、前沿技术的直播讲座,场场爆满,人气过万。最近的一场是关于临床科研课题设计思路之肿瘤免疫抑制的,获得听众们的好评和高度认可,那么下面我们就来简单回顾一下这不到一小时的一节课是怎么介绍国自然课题设计的,还能搭上肿瘤免疫抑制的热点顺风车。
第一部分 临床科研课题设计思路
经过吉凯基因一帮博士们几年的积累,我们总结出一个临床科研课题的研究模式,就是:A 基因通过调控 B 信号通路影响 C 疾病的 D 功能。这个模式对于做科研的老师来说肯定是不陌生的,这个模式下,课题的研究内容主要包括筛选具有临床相关性的 A 基因,A 基因的功能,以及 A 基因的作用机制。与临床相关的 A 基因包括与疾病发生发展相关的基因表达异常,或者突变、或者修饰异常等,所以我们可以从基因组、基因组表观遗传、转录组、蛋白质组层面,从与临床问题相关的组织样本中筛选 A 基因。紧接的第二块内容要研究 A 基因的功能,根据临床问题选择合适的细胞模型和动物模型,进行功能研究。找到 A 基因,也确认 A 基因有功能了,下面就是要进行机制研究了,机制研究也是体现整个课题深度的部分,所以在一个课题中的占比是非常大的,所以下面就来重点介绍下机制研究思路。
从机制研究的深度上来说,机制研究模式分为三大类:第一类分子相关性研究,也即 A 基因改变后,导致下游 B 机制的改变,可以是 B 的表达改变、修饰改变,也可以是空间定位改变。要找下游 B,可以通过查文献,广撒网,找明星通路做验证,这种方式简单,但是可能需要多次尝试,而且创新性也不高。而随着对研究不断深入的需求,通过组学的技术比如测序、蛋白质组等技术方法分析 A 基因的下游分子,通过生信分析来解决机制的方向性问题,成为了很多高分文章采用的方法。找到改变的下游,那么 A 真的是通过 B 来行使功能嘛?
为了解答这个问题,就要进行第二类机制研究,功能相关性分析,主要采用的手段就是功能回复实验。举个例子,A 基因下调,细胞表现出功能改变,而且 A 下调使 B 基因表达也下调,那么把 A 基因下调的同时,把 B 基因上调,通过功能学检测功能是否被回复,若功能回复了,说明 A 下调的确是通过 B 行使细胞功能调控作用的。
第三类机制研究是直接互作,直接互作包括蛋白与蛋白、蛋白与 RNA、蛋白与 DNA、RNA 与 RNA 等,根据 A 基因本身的性质,选择合适的实验方法来进行分析验证,常用的实验方法包括 co-IP,Pull down,RNA-pull down,RIP,ChIP 等。
简单归纳一下一个临床科研课题的思路,如下图:
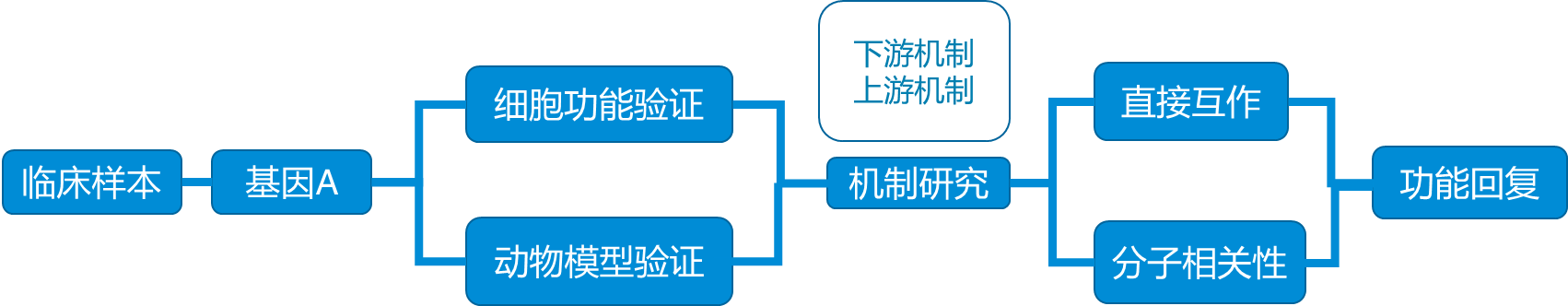
不过这样的文章,内容虽然做的很细致很严谨,但是看起来总觉得平平无奇,就是因为缺少了一些热点,如果能加入一些近期的研究热点就会跟好。那么近期有什么研究热点呢,分析这几年国自然项目,m6A 是这几年大热的方向,也是我们上期直播的主题,感兴趣的老师也可以看我们上一篇文章 (线上直播课网红 m6A RNA 甲基化课题如何设计)。其次就是肿瘤免疫,也是我们接下去要介绍的方向。其他的热点方向还有外泌体、自噬、肠道菌群、干细胞等等,如果我们的研究课题能与这些热点方向联系上,那一定是会增色不少的。
那么下面我们就重点介绍下肿瘤免疫环路与肿瘤免疫治疗。
第二部分 肿瘤免疫环路与肿瘤免疫治疗
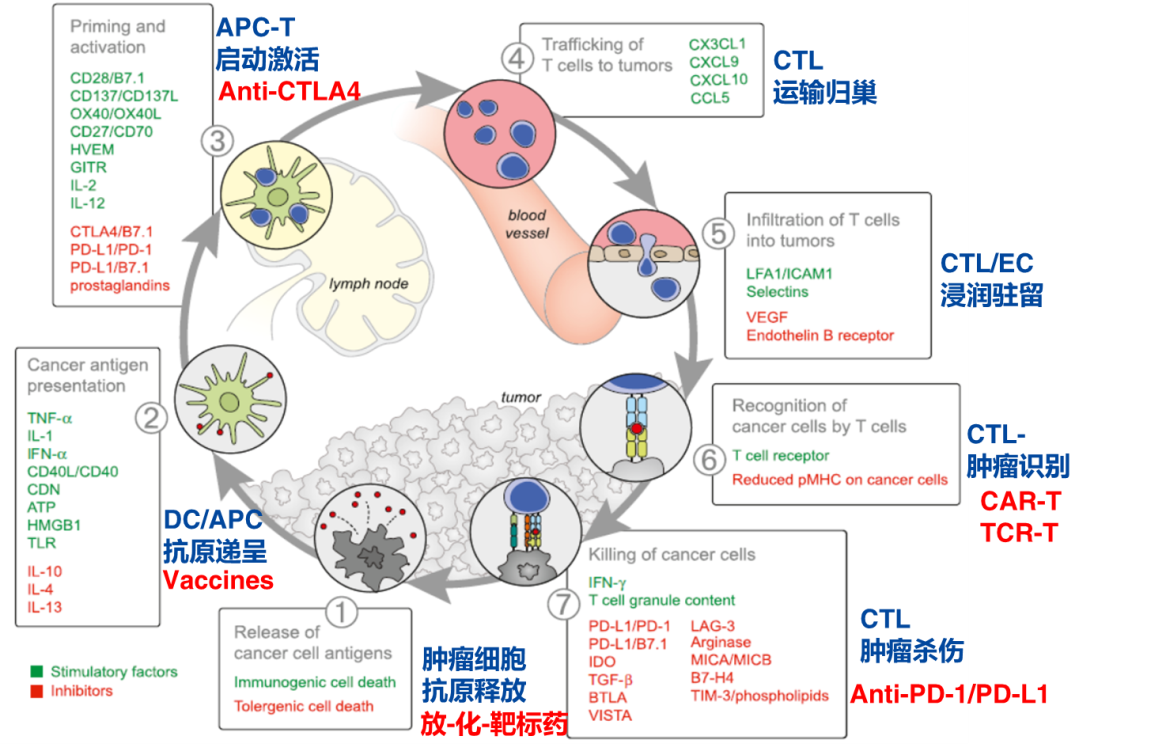
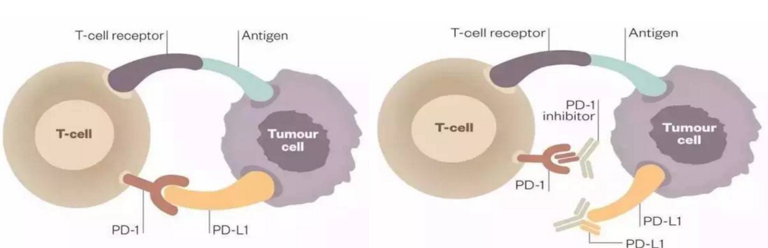
要了解肿瘤免疫和肿瘤免疫治疗,那就需要先了解一下肿瘤免疫环路。在肿瘤免疫环路中,首先肿瘤细胞产生并释放肿瘤抗原,该肿瘤抗原被树突细胞捕获并加工,同时在这个过程中,死去的肿瘤细胞或者菌群会释放炎症因子,产生 T 细胞抗癌效应。接下来 DC 细胞等 APC 细胞将捕获的抗原加功递呈到 T 细胞,启动和激活效应 T 细胞。激活的效应 T 细胞运输并浸润肿瘤组织,通过 T 细胞受体 TCR 以及与 MHCI,识别并结合肿瘤细胞,从而杀死靶细胞,杀死癌细胞会释放出更多的肿瘤相关抗原,使肿瘤免疫环路不断循环。几轮下来,肿瘤就被消灭了,而且有些 T 细胞会转化成记忆细胞,随时可以机动快速地扑灭肿瘤细胞的反复。然而,哪里有压迫哪里就有反抗。肿瘤细胞又具有基因组不稳定的特点,在免疫系统杀伤的生存压力下,有些细胞不断突变进化,逐渐具有了对抗免疫系统的能力,比如不表达新抗原,抗原无法递呈,对 INF-gamma 信号不敏感,表达更多免疫抑制分子 PD-L1 等。这时候,敏感的肿瘤细胞不断被消灭,不敏感的逐渐增多,肿瘤就不断增殖恶化。在这个肿瘤免疫循环中,针对不同环节发生的异常,目前也有一些治疗手段可以实施。比如在抗原递呈阶段,我们可以借助肿瘤疫苗促进抗原递呈,肿瘤识别阶段我们可以通过 CART、TCRT,增加靶向肿瘤的激活 T 细胞,在肿瘤杀伤阶段,通过 PD-1/PD-L1 抑制剂,阻止肿瘤免疫抑制的发生。
那么下面我们就重点介绍下肿瘤免疫环路与肿瘤免疫治疗。
第二部分 肿瘤免疫环路与肿瘤免疫治疗
要了解肿瘤免疫和肿瘤免疫治疗,那就需要先了解一下肿瘤免疫环路。在肿瘤免疫环路中,首先肿瘤细胞产生并释放肿瘤抗原,该肿瘤抗原被树突细胞捕获并加工,同时在这个过程中,死去的肿瘤细胞或者菌群会释放炎症因子,产生 T 细胞抗癌效应。接下来 DC 细胞等 APC 细胞将捕获的抗原加功递呈到 T 细胞,启动和激活效应 T 细胞。激活的效应 T 细胞运输并浸润肿瘤组织,通过 T 细胞受体 TCR 以及与 MHCI,识别并结合肿瘤细胞,从而杀死靶细胞,杀死癌细胞会释放出更多的肿瘤相关抗原,使肿瘤免疫环路不断循环。几轮下来,肿瘤就被消灭了,而且有些 T 细胞会转化成记忆细胞,随时可以机动快速地扑灭肿瘤细胞的反复。然而,哪里有压迫哪里就有反抗。肿瘤细胞又具有基因组不稳定的特点,在免疫系统杀伤的生存压力下,有些细胞不断突变进化,逐渐具有了对抗免疫系统的能力,比如不表达新抗原,抗原无法递呈,对 INF-gamma 信号不敏感,表达更多免疫抑制分子 PD-L1 等。这时候,敏感的肿瘤细胞不断被消灭,不敏感的逐渐增多,肿瘤就不断增殖恶化。在这个肿瘤免疫循环中,针对不同环节发生的异常,目前也有一些治疗手段可以实施。比如在抗原递呈阶段,我们可以借助肿瘤疫苗促进抗原递呈,肿瘤识别阶段我们可以通过 CART、TCRT,增加靶向肿瘤的激活 T 细胞,在肿瘤杀伤阶段,通过 PD-1/PD-L1 抑制剂,阻止肿瘤免疫抑制的发生。
在肿瘤免疫治疗过程中,最终都是落到效应 T 细胞的功能上。naiveT 细胞在暴露于抗原并被其激活后,短期记忆 T 细胞可以增殖并分化为效应 T 细胞,效应记忆 T 细胞,和细胞毒性 T 细胞。随着抗原慢性暴露,效应 T 细胞逐渐耗竭;而且在这一过程中,炎症因子 INF-γ 会刺激 T 细胞表达 PD-1,刺激肿瘤细胞以及其他免疫细胞表达 PD-L1,进一步加剧免疫抑制,而且部分高表达 PD-1 的 T 细胞逐渐发展成不可逆的耗竭 T 细胞,因此整个免疫激活耐受平衡逐渐向免疫抑制方向倾斜。而这其中 PD-1/PD-L1 通路的影响非常大。根据对肿瘤免疫环路以及肿瘤免疫耐受平衡的了解,肿瘤免疫治疗其实可以归为两大类,一类就是通过增强免疫,来杀伤肿瘤,包括细胞因子刺激 T 细胞、CTLA4 抗体促进 T 细胞激活,以及近年来也非常火热的 CAR-T/TR-T 治疗;另一类免疫治疗主要是使免疫正常化,去除肿瘤微环境中的免疫抑制,这其中目前研究的最多的免疫抑制通路就是 PD-1/PD-L1 了。而且 PD-1/PD-L1 具有广谱性,目前通过 FDA 批准的针对 PD-1/PD-L1 的药物已在多个癌种中有应用。
虽然 PD-1/PD-L1 是目前研究最多的肿瘤免疫抑制通路,但是 PD-1/PD-L1 抑制剂在临床上的应用仍有很多问题很多挑战,第一个问题就是如何提高响应率,PD-1/PD-L1 的总体响应率在 10-40%,还是比较低的;第二个就是如何延长相应时间;第三个是如何抵抗 PD-1/PD-L1 抑制剂耐药。要解决这些问题,需要筛选更有效的 PD-1/PD-L1 抑制剂优势人群的生物标志物,研究 PD-1/PD-L1 抑制剂使用时机以及与其他治疗方式的联合应用,这些工作需要更多的临床研究数据。当然,针对 PD-1/PD-L1 的通路机制研究也是少不了的,只有更深入了解了 PD-1/PD-L1 通路机制,才能为临床应用提供更好的理论依据。所以下面我就来看下以 PD-1/PD-L1 为切入点我们该怎么去做研究。
第三部分肿瘤免疫抑制设计思路
针对 PD-1/PD-L1 的国自然课题以及文献数每年都在快速增加,所以我们又拉了这两年中标的国自然课题,去分析这些课题都在进行哪些研究,发现以 PD-L1 为研究对象的课题,我们也可以用一句话给概括出来,就是:A 基因通过 B 机制调控 PD-L1 影响 C 疾病的免疫抑制 / 免疫治疗。这个模型是不是和前面第一部分介绍的 A-B-C-D 的研究模式非常相似,只不过在这一类课题里,功能是目前研究火热的和 PD-L1 相关的肿瘤免疫抑制。那么针对 PD-L1 的调控机制,其实小编在我们之前的一篇文章里 (还在找研究热点,不如看看您做的基因是否和 PD-L1 相关?) 也有过介绍,在那篇文章里,我们介绍了 PD-L1 的而表达以及功能可以在 5 个层面受到调控:
- 基因组层面的拷贝数突变或者表观遗传修饰;
- 癌基因通路或炎症因子通路等对 PD-L1 的转录调控;
- miRNA 等对 PD-L1 mRNA 水平的调控,以及翻译调控;
- 翻译后调控,蛋白水平上的修饰如:乙酰化、泛素化、磷酸化、糖基化、棕榈酰化等;
- PD-L1 通过可溶性蛋白形式或者外泌体包裹形式到达胞外行使功能。
综上,PD-L1 可以受到多方多形式的调控行使免疫抑制功能,就看我们的目的基因会是否会以及如何影响 PD-L1 了。下面我们就以两篇文章为例简单介绍下关于 PD-L1 的研究。
文献一:

2017 年的一篇 Nature 通过 CRISPR-cas9 文库筛选到一个会影响 PD-L1 上膜的分子 CMTM6。作者首先通过 CAS9 文库感染肿瘤细胞,通过流式筛选膜上低表达 PD-L1 的细胞,将筛选出的细胞进行 sgRNA 测序,发现 CMTM6 的敲除可以显著影响 PD-L1 的细胞膜上表达。
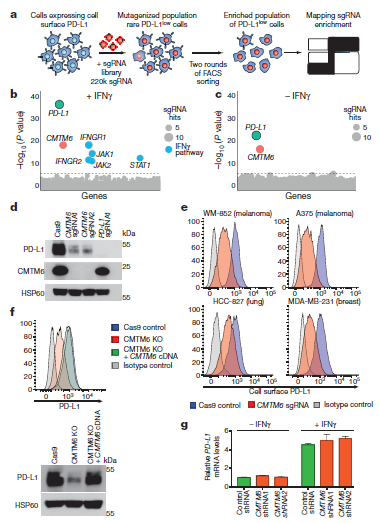
随后通过 co-IP、膜蛋白 TMT 蛋白质组、蛋白失踪实验等机制研究,发现 CMTM6 与 PD-L1 互作,且与其内吞循环过程相关。这个部分研究主要就是进行了机制研究(直接互作、分子相关性、功能回复)。那么 CMTM6 影响 PD-L1 上膜,是否会影响到肿瘤免疫抑制,接着作者就用 CMTM6 敲除的肿瘤细胞与 T 细胞共培养,检测 CD8+perforin+T, CD8+TNFα+T 细胞比例,以及 IFN γ 和 IL-2 的分泌检测,判断 CMTM6 敲除的肿瘤细胞对 T 细胞的激活影响,同时运用免疫健全小鼠进行成瘤模型构建,验证 CMTM6 对肿瘤免疫抑制的影响。
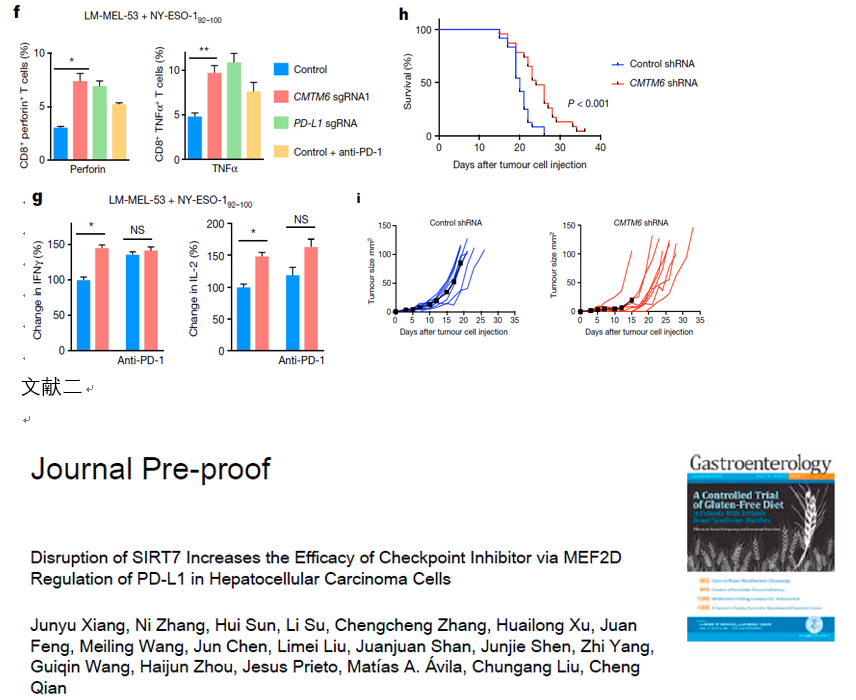
这篇是 2020 年发表在 Gastroenterology(19.233)上的文章。
这篇文章的第一个实验是通过免疫组化实验发现 MEF2D 表达与组织中 CD4+,CD8+T 细胞比例呈负相关,与 PD1 + 和 TIM3 + 的 CD8+T 细胞(耗竭 T 细胞)呈正相关,表明该基因可能与肿瘤免疫相关。
这篇文章的第一个实验是通过免疫组化实验发现 MEF2D 表达与组织中 CD4+,CD8+T 细胞比例呈负相关,与 PD1 + 和 TIM3 + 的 CD8+T 细胞(耗竭 T 细胞)呈正相关,表明该基因可能与肿瘤免疫相关。
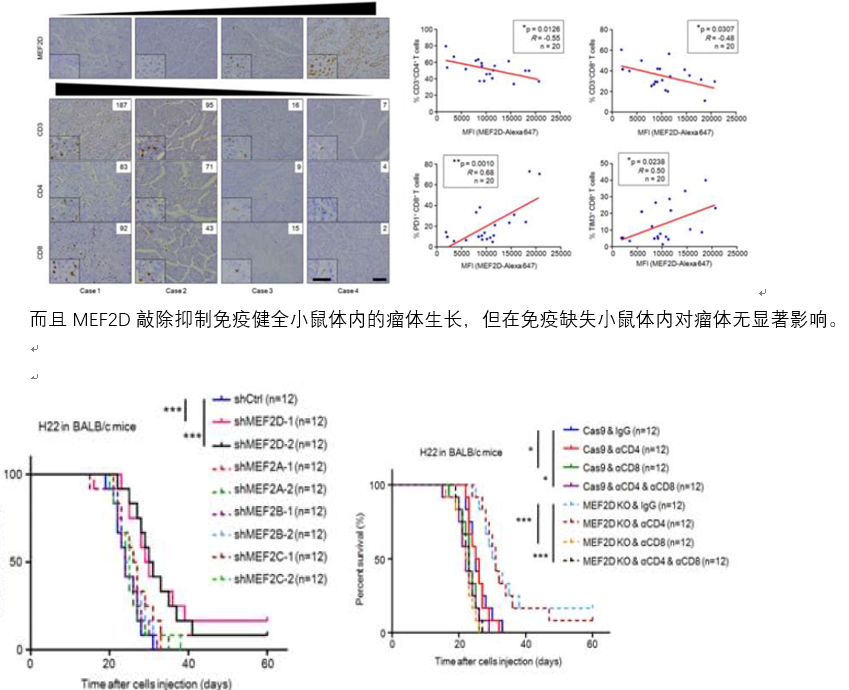
初步发现临床相关性和和动物功能之后,作者通过 RNA-seq,ChIP, luciferase 实验验证 MEF2D 可调控 PD-L1 的转录。通过将 PBMC 与 MEF2D 敲除的肿瘤细胞共培养,检测 CD8+TNFα+T 细胞数量、IL2\IFNγ 分泌,以及免疫健全小鼠进行成瘤模型构建,确认 MEF2D 敲除的确会促进 T 细胞的激活,去除肿瘤免疫抑制,但是 MEF2D 对肿瘤的生长并无影响。
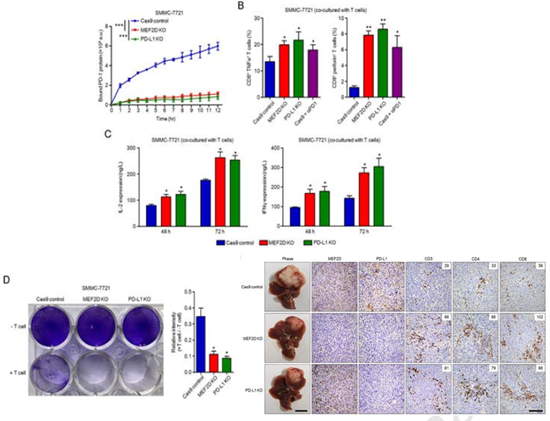
作为一篇将近 20 分的文章,研究内容肯定不能这么简单,所以作者通过 co-IP,ChIP/Re-ChIP 等一些列实验发现 p300、SIRT7 介导 MEF2D 乙酰化调控了 PD-L1 的表达,找到了 MEF2D 的上游分子。而且通过肿瘤细胞与 T 细胞共培养模型以及免疫健全小鼠成瘤模型发现,SIRT7 抑制了 T 细胞的激活,促进肿瘤免疫抑制。而 MEF2D 敲除可回复 SIRT7 敲除引起的免疫抑制作用。但同时,SIRT7 敲除本身又可抑制肿瘤细胞体外增殖以及体内瘤体生成。看来 SIRT7 可以既调控 MEF2D 对 PD-L1 的调控,也可以影响肿瘤细胞的增殖,是一个潜在治疗靶点。所以最后,作者又将 SIRT7 敲除与 PD-1 抗体联用,在小鼠成瘤模型上验证治疗效果。
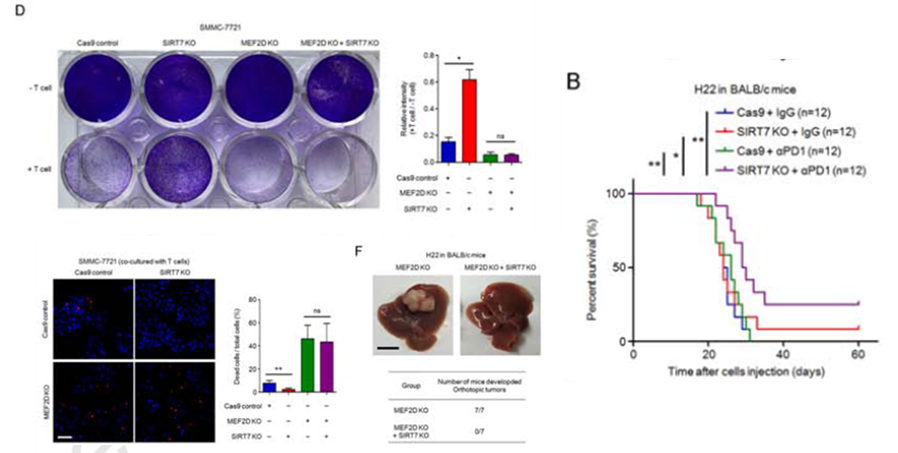
所以这样的一个研究,既与目前的研究热点相关,又与临床治疗相联系,既具有基础研究意义,又有临床研究意义,是一定能发高分的文章的。
总结一下这两篇与肿瘤免疫抑制相关的文章思路:
总结一下这两篇与肿瘤免疫抑制相关的文章思路:

研究思路是类似的,找到 A 基因,验证 A 基因是否可能调控 PD-L1,从而影响肿瘤免疫抑制。解下来您知道该怎么做了吧。
如果您还没有 A 基因,那也不用着急,吉凯基因历经 3 年,斥资上亿,完成近 6000 个肿瘤相关基因的功能学筛选,已从中找到明确的新的肿瘤关键功能基因 —— 潜在的药靶基因若干,等您来寻宝~~
参考文献:
- The deubiquitylase OTUD3 stabilizes GRP78 and promotes lung tumorigenesis. NATURE COMMUNICATIONS | (2019) 10:2914
- Disruption of SIRT7 Increases the Efficacy of Checkpoint Inhibitor via MEF2D Regulation of PD-L1 in Hepatocellular Carcinoma Cells. Gastroenterology, 158 (3), 664-678.e24
- CMTM6 maintains the expression of PD-L1 and regulates anti-tumour immunity. Nature, 549 (7670), 101-105. 2017 Sep 7
- Oncology Meets Immunology: The Cancer-Immunity Cycle. Immunity, 39 (1), 1-10. 2013 Jul 25