上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
公司新闻/正文
干货!打好这个基础,「小非编码RNA」研究一点都不难
955 人阅读发布时间:2020-08-24 15:37
随着二代测序技术的发展,研究人员发现人类基因组中90%的RNA转录本不会转录成蛋白。这些所谓的非编码RNA的功能和多样性都非常复杂,涉及到细胞增殖、分化、凋亡、代谢等多个生物过程。其中,对于不超过400个核苷酸(nt)的非编码RNA,被重新分类为小非编码RNA(small non-coding RNA,sncRNA)。我们经常听到的miRNA即属于小非编码RNA。本文将详细地介绍miRNA和tiRNA(tRF)两类小非编码RNA的生物发生和功能。
miRNA的生物发生和功能
1993年,Ambros在线虫中克隆了lin-4基因,并通过定点突变发现lin-4并不编码蛋白,而是产生一种小RNA分子。这种小RNA分子能以不完全互补的方式与其靶向mRNA的3‘UTR的特定区域相互作用来抑制lin-14的表达,最终导致lin-14蛋白质合成减少,这种现象叫做转译抑制。lin-4控制着线虫幼虫由L1期向L2期的转化【1】。从此之后,开始揭开了miRNA的研究序幕。
所谓miRNA(microRNA),是一种不编码蛋白质,大小约18-24nt的单链小分子RNA,它具有在翻译水平或者转录水平调控基因表达的功能。目前发现miRNA最主要的功能是结合靶标mRNA的3’UTR,抑制翻译过程的进行。
由于miRNA的研究已经非常成熟,所以其合成的途径现在也已经研究得比较清楚。下面为大家作简要介绍。
在经典miRNA合成途径中,最开始转录的pri-miRNA在核内被Drosha及其辅助因子Pasha加工,形成60-110nt左右具有颈环结构的pre-miRNA。该pre-miRNA随后被exportin 5转运至细胞质,并被Dicer切除环状序列,形成~22nt双链的RNA,随后形成了RNA诱导的沉默复合物(RISC),这一过程即miRNA的成熟过程(图1)。
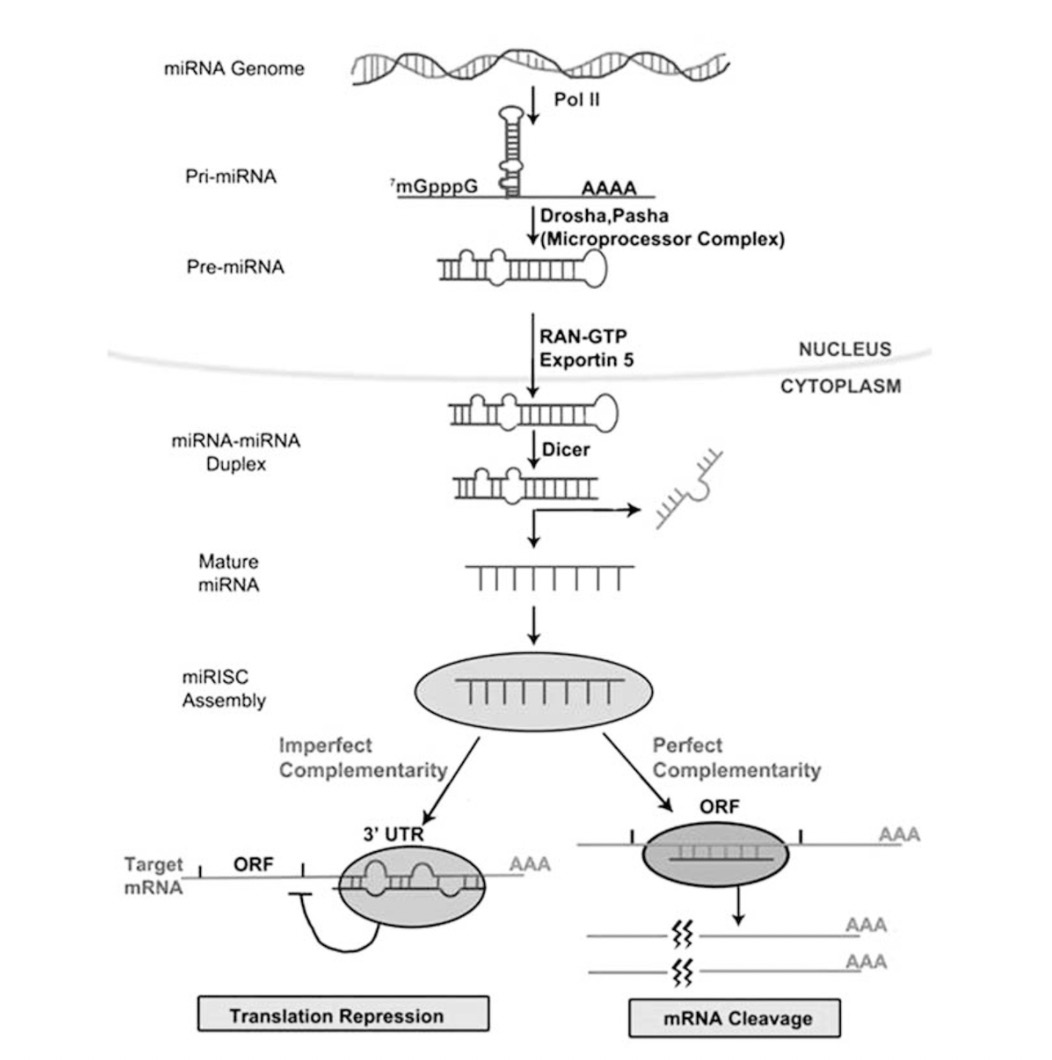
图1. miRNA合成过程
在形成RISC过程中,一个非常重要的蛋白是AGO2。现在一般认为AGO2参与了形成RISC过程中后随链的降解。所谓后随链就是前面提及双链RNA未参与形成RISC的一条链。并且,当miRNA与靶标mRNA完全互补结合之后,AGO2也将参与靶标mRNA的切割。相对的,当miRNA与靶标mRNA不完全互补结合,会抑制靶标mRNA的翻译过程【2】。
在了解miRNA的成熟过程之后,我们很容易联想到一个问题,Dicer切割后形成的双链RNA,到底是选择正义链还是选择反义链成为成熟的miRNA呢?如果对miRNA有所了解,那你可能知道,选择不同链的结果是大相径庭的。Schwarz及其同事通过在体外合成不同结构的双链RNA,检测其两条链不同的成熟比例。发现miRNA成熟过程链的选择并不是随机,而是会选择5’ 端不稳定的链作为向导链(miRNA成熟链)(图2),简单来说,RISC复合物更倾向于选择5’端AT含量更高,或者5’端有错配的链作为向导链【3】。
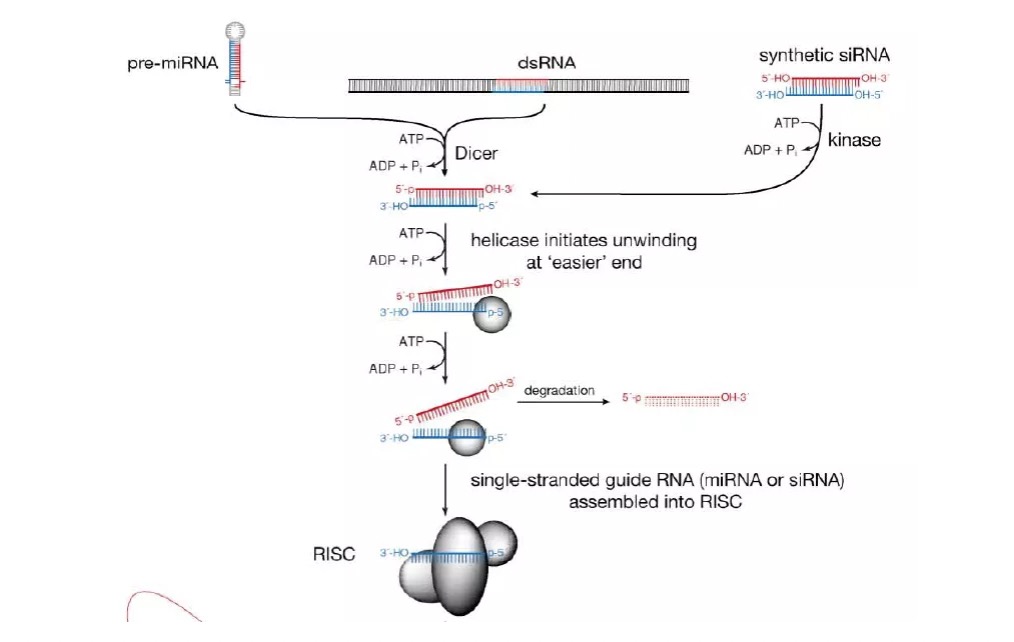
图2. miRNA向导链的选择
前面有提到miRNA的一个主要功能是结合靶标mRNA的3’UTR,抑制翻译过程。那么这一功能是怎样实现的?目前研究主要有三条通路(图3)。
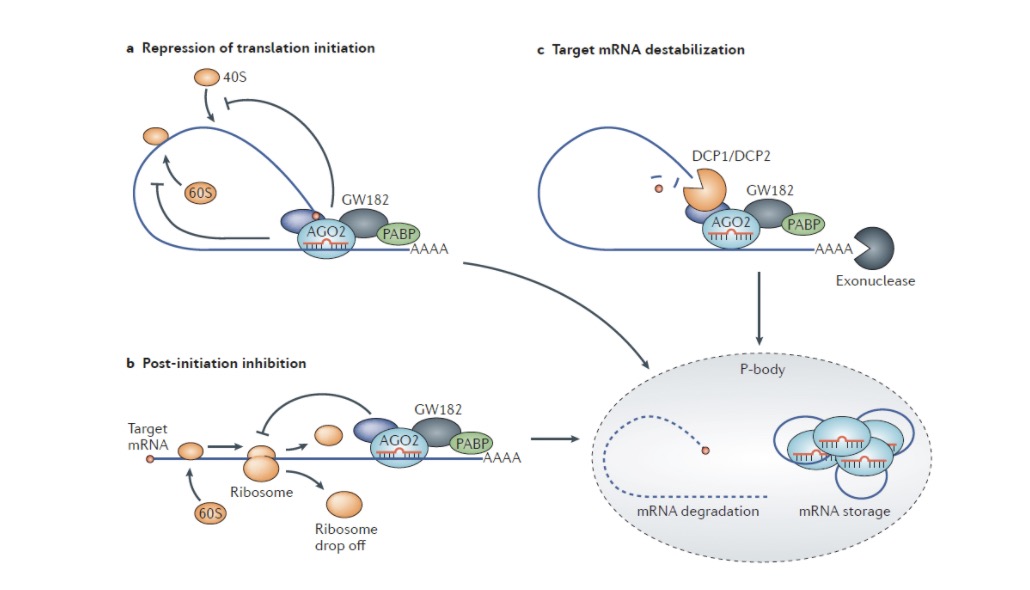
图3. miRNA对mRNA的调节过程
第一条通路,通过抑制真核生翻译起始因子4F(eIF4F)对mRNA的5’帽子的识别,抑制40s和60s核糖体亚基的招募,阻止80s核糖体复合物的形成。
第二条通路,RISC可能会抑制核糖体复合物在mRNA链上的延伸,导致这些核糖体复合物从mRNA上脱落,最终未成功翻译的多肽将被降解。
第三条通路,RISC通过招募mRNA去帽子的酶,降低mRNA的稳定性,影响其翻译起始过程【3】。
tiRNA的生物发生和功能
tRNA的主要功能是在蛋白合成过程进行氨基酸的转运。成熟的tRNA长度在79nt左右,并在3’端携带一个氨基酸。tRNA的二级结构是个经典的3叶草结构,包含有3个颈环结构(D环、T环和反密码子环)。人类基因组中有多达506个基因编码49个不同的tRNA。tRNA被polymerase III转录。Pre-tRNA具有和成熟tRNA类似的二级结构,还包含有额外的5’端引导序列和3’端拖尾序列。在后续成熟过程中这两段序列均会被切除,并且3‘端还会被额外添加5’-CCA-3‘,该序列对于tRNA转运氨基酸是必需的。
并且,在成熟过程中tRNA还会经历一系列的转录后修饰,这些修饰将影响tRNA的构象、稳定性和功能。最终在被20种不同的氨基酰化合成酶催化发生氨基酰化之后,成熟的tRNA被Exportin-T从细胞核转运至胞质,参与蛋白合成过程【4】。
高通量测序分析发现了一类新的小非编码RNA。通过比对,该类RNA可以比对到tRNA的基因,这类RNA被命名为tiRNA(tRNA halves)或者tRF(tRNA-related fragment)。根据比对到成熟tRNA转录本的不同位置,tiRNA和tRF被分成了不同的类别(图4)。比如,在反密码子处切割,产生两种tiRNA。从成熟tRNA的5’末端至反密码子结束的片段被称为5‘tiRNA,从反密码子开始至成熟tRNA的3’末端的片段被称为3’tiRNA。这两类分子的大小在29-50nt左右。需要注意的是5‘tiRNA和3’tiRNA的成熟依赖的angiogenin的切割而不是Dicer,其5’端具有羟基而不是磷酸。
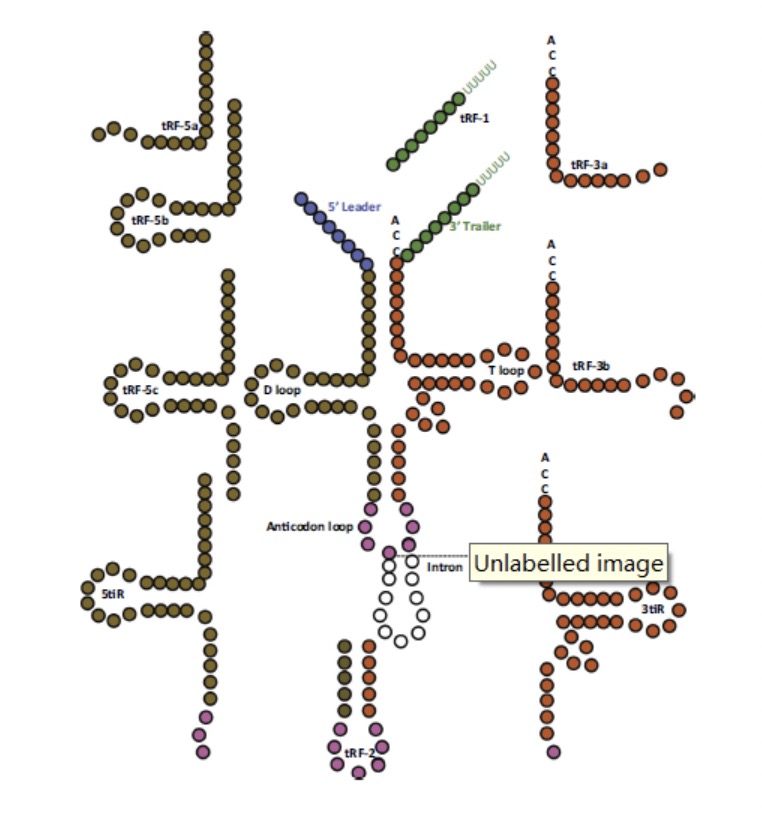
图4. tRF的分类
还有一类来源于tRNA的小RNA,长度在14-30nt左右,含有5’端的磷酸和3‘的羟基。根据他们在tRNA上的比对位置,这些小RNA被分成4类:tRF-5、tRF-3、tRF-2和tRF-1。其中tRF-5和tRF-3分别对应tRNA的5’端和3’端。而另外两个特殊的tRF中,tRF-2是只包含有tRNA反密码子的一个小RNA片段,tRF-1则源于pre-tRNA的3’端拖尾序列【5】。
那么,各类tRF和tiRNA是被如何调控和成熟的?又是通过何种方式发挥其功能的呢?这两个问题目前都还覆有阴影,但是从现有的一些研究结果依然可以管中窥豹。比如,虽然目前发现的绝大部分tRF5和tRF3的成熟都被发现与Dicer无关,但是他们之中相当多的一部分却被发现与Ago家族的蛋白,尤其是Ago1、3、4有着很强的关联。通过光活性增强的核糖核苷交联和免疫共沉淀(PAR-CLIP)实验有力地证明tRFs能够进入到Ago复合物,并通过种子序列区域同靶向mRNA结合,这种结合类似于miRNA-AGO-mRNA复合物模式。这暗示了tiRNA可能存在的类似miRNA的调控机制。
目前研究发现的tRF涉及的生物学功能非常广泛,包括抑制转录、调控组蛋白修饰、抑制RPA1导致细胞周期抑制、促进或者抑制肿瘤增殖、抑制渗透压力导致的细胞凋亡等等。
相对于miRNA的研究成熟,tRF无论是成熟通路还是发挥功能的具体调控机制都还有太多的未知,还需要更多的探索。
小 结
对于非编码RNA的研究愈来愈有力地证明,对于诸多生物学功能,包括细胞增殖、分化、命运决定、表观遗传修饰改变、肿瘤发生和抑制等,非编码RNA或者可以说小非编码RNA才是那个背后最终调控的神秘之手。越来越多原先被认为是转录副产物的一些非编码RNA被发现具有新的功能,miRNA、circRNA、piRNA、tiRNA等无不如此,均是在近10年或者20年内发现的。
可以预见,在不远的将来,必将有更多种类的小非编码RNA被发现,而这将进一步改变我们对基因表达调控的理解。例如,基因组上的大量异染色质区域真的不会发生转录吗?是否存在一种可能,某个异染色区域存在低程度的转录,而由于异染色质上大量的异染色质marker,如H3K27me3,会导致这种转录提前异常中止。而这类提前中止的转录本后续会被剪切成某类小非编码RNA。如果把编码基因看成有限区间内的整数,我们会发现,未被发现的整数已经越来越少了;但是如果将非编码RNA看成这个区间内的小数,其背后隐藏的宝藏或许远超我们的想像。
吉凯基因拥有丰富的调控非编码RNA方案设计的经验,如果大家对这方面的信息感兴趣,欢迎扫码咨询。