上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
公司新闻/正文
miRNA 下调新方法:教你如何摆脱 QPCR 检测无效
3197 人阅读发布时间:2020-11-18 13:20
miRNA 作为热门的小 RNA 分子,已经在科研圈火了很多年,尤其是 lncRNA、circRNA 的海绵机制被发现后,作为 ceRNA 的核心,又变得炙手可热。基于 miRNA 的功能缺失手段也较为成熟,但是不少实验者反馈:「做 miRNA 下调,QPCR 检测 miRNA,表达水平无变化」,这到底是怎么回事、以及如何解决呢?
一、miRNA 抑制为啥
QPCR 检测无效?
现有 miRNA 抑制手段,无论是基于载体构建的、还是化学合成的,本质上都是用跟成熟体互补的反义 miRNA(miRNA 海绵体属于不完全互补的反义 RNA 重复),其可以通过结合 miRNA,阻断其与靶基因结合,但并不能有效引发 miRNA 的降解,原因有两方面:其一是反义 RNA 与 miRNA 结合后,序列很短,导致 Dicer 酶(细胞内降解双链 RNA 的主角)不能有效结合;其二是 miRNA 与 Ago2 以 RISC 复合物的形式存在,该复合物也会导致 Dicer 酶无法高效结合。
首先,我们看下《RNA Biology》上一篇文章对于 miRNA 反义核酸的描述1:
首先,我们看下《RNA Biology》上一篇文章对于 miRNA 反义核酸的描述1:

翻译一下:

因此,如果以反义 RNA 技术抑制 miRNA 功能,QPCR 可以做,如果检测出表达水平下降还好,即便未检测到,也不表示抑制无效,正确的做法是直接检测目的基因蛋白水平是否有上调。但若实验者不清楚靶基因的情况下,不检测到 miRNA 下调,心里是没底的,如何解决呢???
反义核酸是在转录后水平发挥功能,要阻断 miRNA 的产生,理想情况是在生成成熟的 miRNA 之前阻断。此要求目前唯有 CRISPR / Cas9 能实现,Cas9 通过在 pre-miRNA 序列中引入突变,从而破坏 miRNA 表达,是 miRNA 基因功能缺失研究的一种新方法。
反义核酸是在转录后水平发挥功能,要阻断 miRNA 的产生,理想情况是在生成成熟的 miRNA 之前阻断。此要求目前唯有 CRISPR / Cas9 能实现,Cas9 通过在 pre-miRNA 序列中引入突变,从而破坏 miRNA 表达,是 miRNA 基因功能缺失研究的一种新方法。
二、CRISPR / Cas9 敲除
miRNA 案例
CRISPR / Cas9 能实现miRNA 的敲除吗?技术会被认可吗?
首先,列举两篇运用吉凯基因 Cas9 病毒实现 miRNA-KO 的文章:
福建肖老师运用 Cas9 技术,针对 miR-21 基因设计 sgRNA ,通过慢病毒递送细胞,并在 RNA 水平检测到 mir-21 的下调表达,从而研究出 miR-21 耗竭对 CNE2 鼻咽癌(NPC)细胞生物学特性及其潜在机制的影响2。
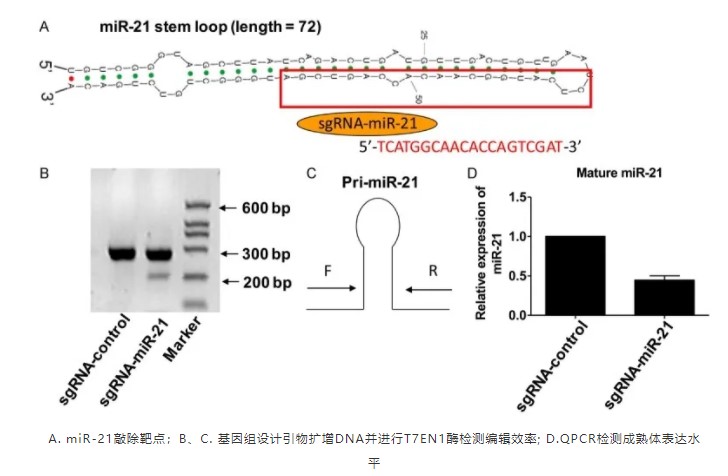
使用 Cas9 敲除 miR-21 之后,功能上也呈现出阳性:
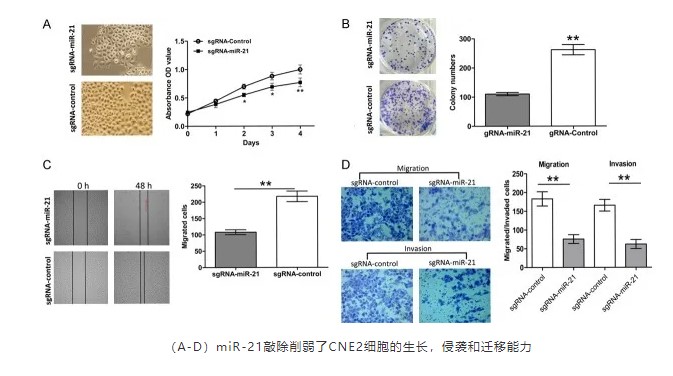
此外,温医大第一医院的张老师使用 Cas9 敲除 mir-545,研究了人环状 RNA PRKCI(circPRKCI)通过抑制 miR-545 显示致癌性,促进人类神经胶质瘤细胞的病理进展3。
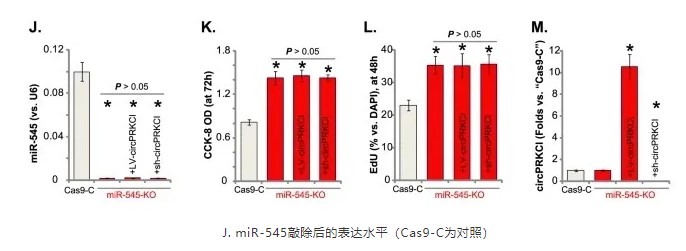
所以,CRISPR / Cas9 对于 miRNA 的 KO 是有效的、被认可的、且以 QPCR 检测表达量完全没有问题,那该技术内在的机制是怎样的呢?
三、CRISPR / Cas9 敲除
miRNA 的分子机制
首先,从 miRNA 形成机制谈起,前体 pri-miRNA 由基因组转录,该前体一般长约几 KB 至几十 KB 不等,每个 miRNA 的 pri 长度都不一样,pri 在细胞核进行第一次剪切形成 pre 前体,pre 一般长约 70-120bp,含有类似于 shRNA 的颈环结构,pre 随后转运至细胞质,在 Dicer 酶的剪切下变为成熟体。
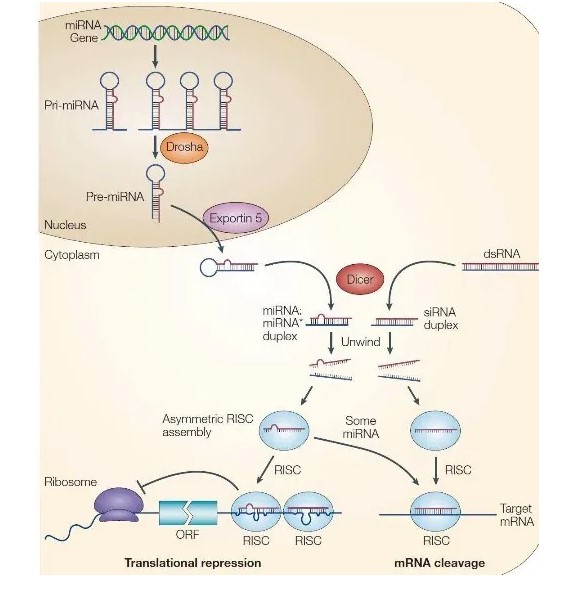
miRNA 成熟过程
针对 pre 前体序列设计 Cas9 靶点,将 DNA 打断后,依靠非同源末端连接(NHEJ) 效应,在 pre 的成熟体或者颈环上引入突变碱基或者缺失,从而破坏颈环整体结构,引发 pre 剪切受阻,从而抑制了成熟体的产生。实验证明,靶点位于颈环或者臂都能有效抑制 Dicer 酶剪切4:
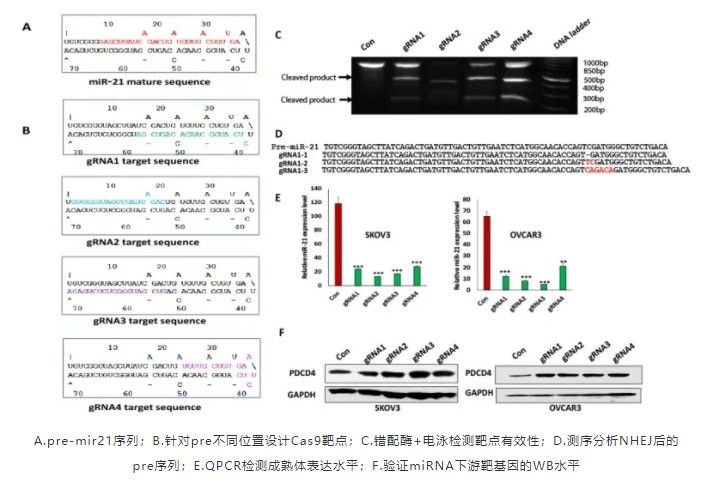
综上所述,Cas9 技术为 piRNA、miRNA 这类小 RNA 分子的抑制提供了除反义核酸之外的另一种选择,并能有效解决 QPCR 检测不稳定的难题。吉凯基因常规针对 pre-miRNA 设计两个 Cas9 靶点定制,80% 的情况下能实现至少一个靶点对 miRNA 的有效 KO,还在等什么,快来咨询吧!!!

吉凯基因,年产上万次慢病毒、腺病毒、腺相关病毒;
建有国内大型的慢病毒文库,包含几乎覆盖人类所有基因的,近 15 万个独立克隆;
国内集产品采购和资讯分享的一体化综合服务平台,为科研工作者提供一键式的采购服务,产品周期短至 5 个工作日起;
18 年品质保证、助力客户发表 10000+ 篇 SCI,多项科研成果发表于 Nature Medicine、Nature Immunology、Gastroenterology、Cell Metabolism、Nature Neuroscience 等著名期刊上
【参考文献】
1. Anti-miRNA oligonucleotides: A comprehensive guide for design.
2. MicroRNA-21 depletion by CRISPR/Cas9 in CNE2 nasopharyngeal cells hinders proliferation and induces apoptosis by targeting the PI3K/AKT/MOTOR signaling pathway.
3. Circular RNA PRKCI promotes glioma cell progression by inhibiting microRNA-545.
4.Lentiviral CRISPR/Cas9 vector mediated miR-21 gene editing inhibits the epithelial to mesenchymal transition in ovarian cancer cells.