上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
公司新闻/正文
SCI TRANSL MED(IF 17):多组学+人工智能揭秘年轻人新冠症状的驱动基因
515 人阅读发布时间:2022-03-18 11:29
2019冠状病毒感染(COVID-19)的临床表现复杂且多样,大致可分为四个类别:(i)无症状的个体;(ii)患者显示流感样疾病;(iii)患者受到呼吸功能障碍,需要外部氧气供应;(iv)表现为急性呼吸窘迫综合征(ARDS),需要在重症监护病房(ICU)进行治疗和护理。虽然最后这个类别仅代表COVID-19患者的一小部分,但其包含了该病最危重的疾病形式,平均病死率约为25%。为什么感染后的病程及临床表现显示出如此大的差异?为什么部分没有任何基础疾病的年轻人也会发展出危重症状?这些问题仍然没有清晰的答案。

近期,多个国家研究团队联合在Science Translational Medicine(中科院JCR一区,IF:17.956)上发表题为“Sci Transl Med: Identification of driver genes for critical forms of COVID-19 in a deeply phenotyped young patient cohort”的研究论文。研究者通过对COVID-19危重组和非危重组的年轻患者进行了全基因组测序、全血RNA测序、血浆和血液单个核细胞蛋白质组学、细胞因子谱分析和高通量免疫表型等分析和验证,并结合人工智能和机器学习等算法找到了一组基因集可有效区分危重和非危重患者,并发现ADAM9是疾病严重程度的驱动因素,或可成为疾病治疗的潜在靶点。
研究思路
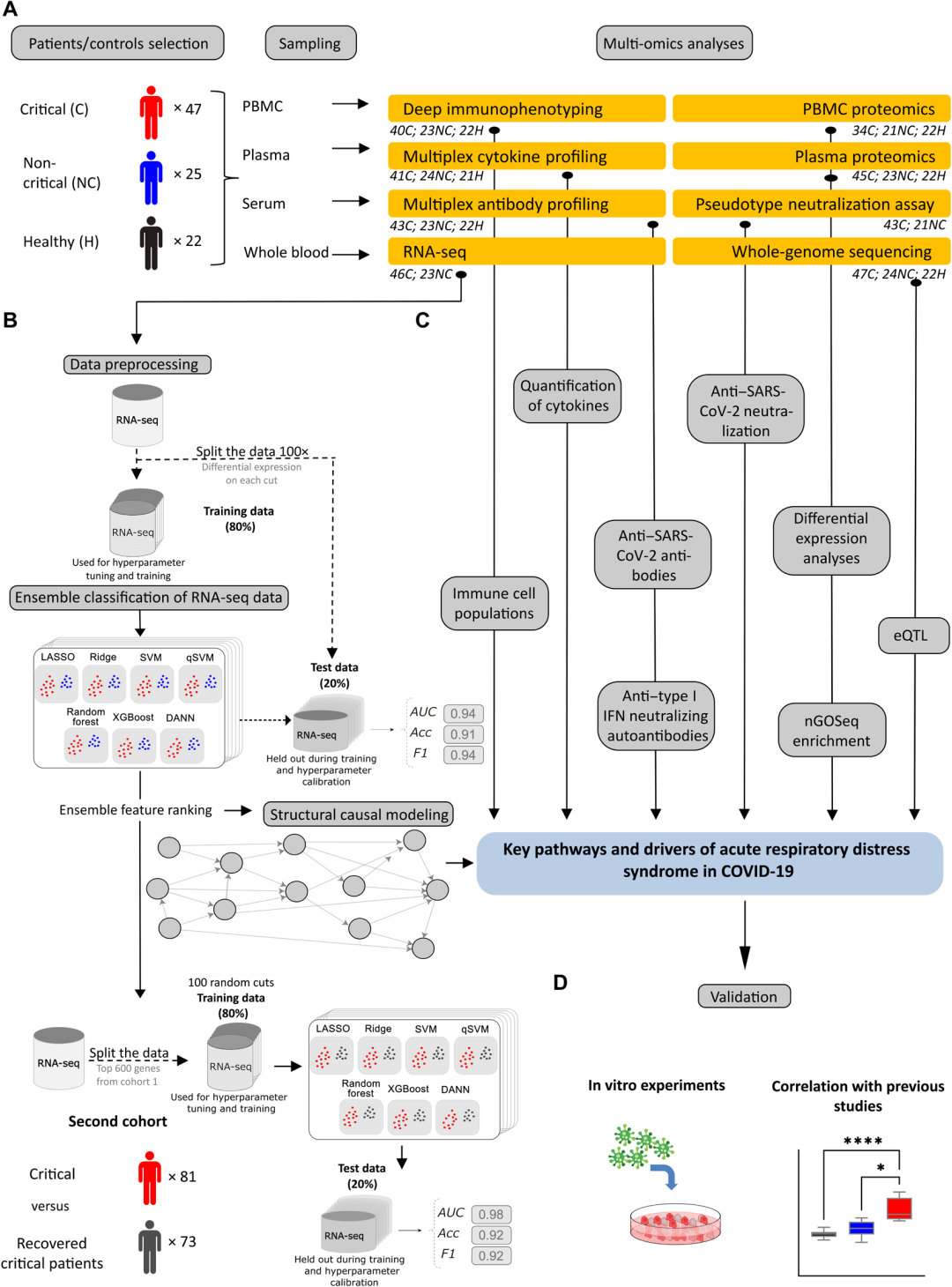
01样本分组设计
(1)第一个独立队列(均为年龄50岁以下的个体):
危重疾病组:47名(平均年龄41)
非危重疾病组:25名(平均年龄38)
健康对照组:22名
(2)第二个独立队列(均为年龄50岁以下的个体):
危重疾病组:81名
已康复的危重疾病组:73名
02多组学技术总结
| 序号 | 样本类型 | 技术 |
| 1 | 全血 | 全基因组测序(WGS) |
| 2 | 全血 | RNA测序 |
| 3 | 全血 | 高通量免疫细胞表型分析 |
| 4 | 血浆 | 蛋白质组学 |
| 5 | 血浆 | 细胞因子谱检测 |
| 6 | 血清 | 抗SARS-CoV-2中和抗体检测 |
| 7 | 血清 | 抗I型干扰素(IFN)中和抗体检测 |
| 8 | 外周血单个核细胞(PBMC) | 蛋白质组学 |
03技术路线
研究结果
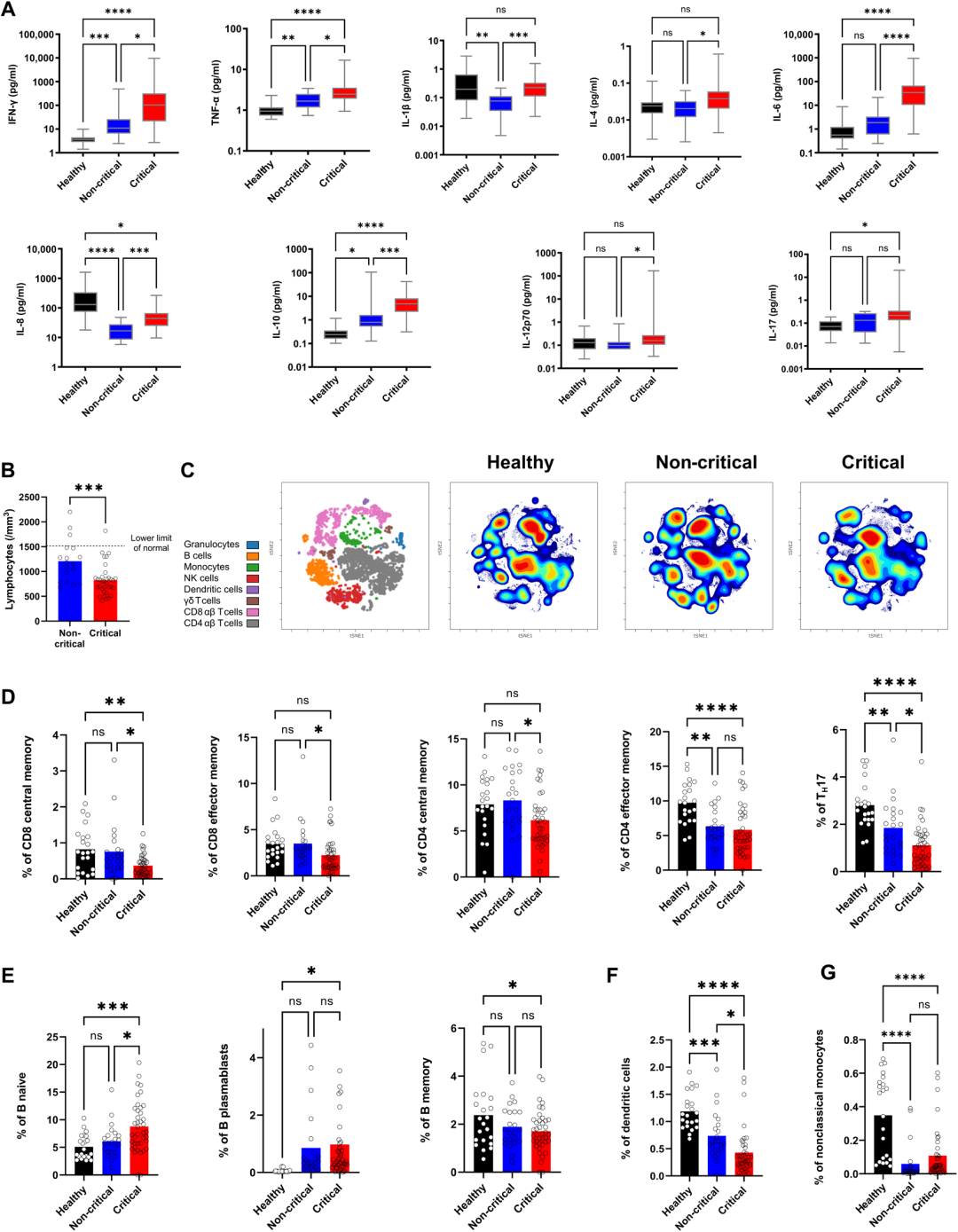
1. 危重疾病的特征是促炎细胞因子风暴和T、B、树突状和单核细胞区室的变化,且与病毒感染的程度无关
促炎细胞因子检测显示,与非危重疾病组相比,干扰素γ(IFN-γ)、肿瘤坏死因子α(TNF-α)、IL-1β、IL-4、IL-6、IL-8、IL-10、IL-12p70在危重疾病组中显著上调。这种“细胞因子风暴”在危重患者中更为明显,因为非危重患者中只有IFN-γ,TNF-α和IL-10高于健康对照组。淋巴细胞减少与疾病的严重程度相关。研究者进一步对血液中分离出的外周血单个核细胞(PBMC)进行了免疫细胞表征,可覆盖37个免疫细胞群。随机邻域嵌入(viSNE)的可视化显示,在危重患者中存在一种特异性的细胞群密度分布模式。这种模式可能与危重患者已知的免疫抑制现象有关,其特征是T细胞区室存在显著差异,记忆性CD4和CD8 T细胞和TH17细胞与疾病严重程度呈负相关。与健康对照组相比,危重患者的B细胞区室包含更多的幼稚B细胞和浆母细胞以及更少的记忆B细胞。此外,非危重症和危重症患者的树突状细胞和非经典单核细胞数量也较少。总之,研究结果表明,危重疾病的特征是促炎细胞因子风暴和T、B、树突状和单核细胞细胞区室的显著变化。这些特异性变化与病毒感染的程度无关,因为抗SARS-CoV-2抗体浓度和中和活性在危重组和非危重组中没有差异。
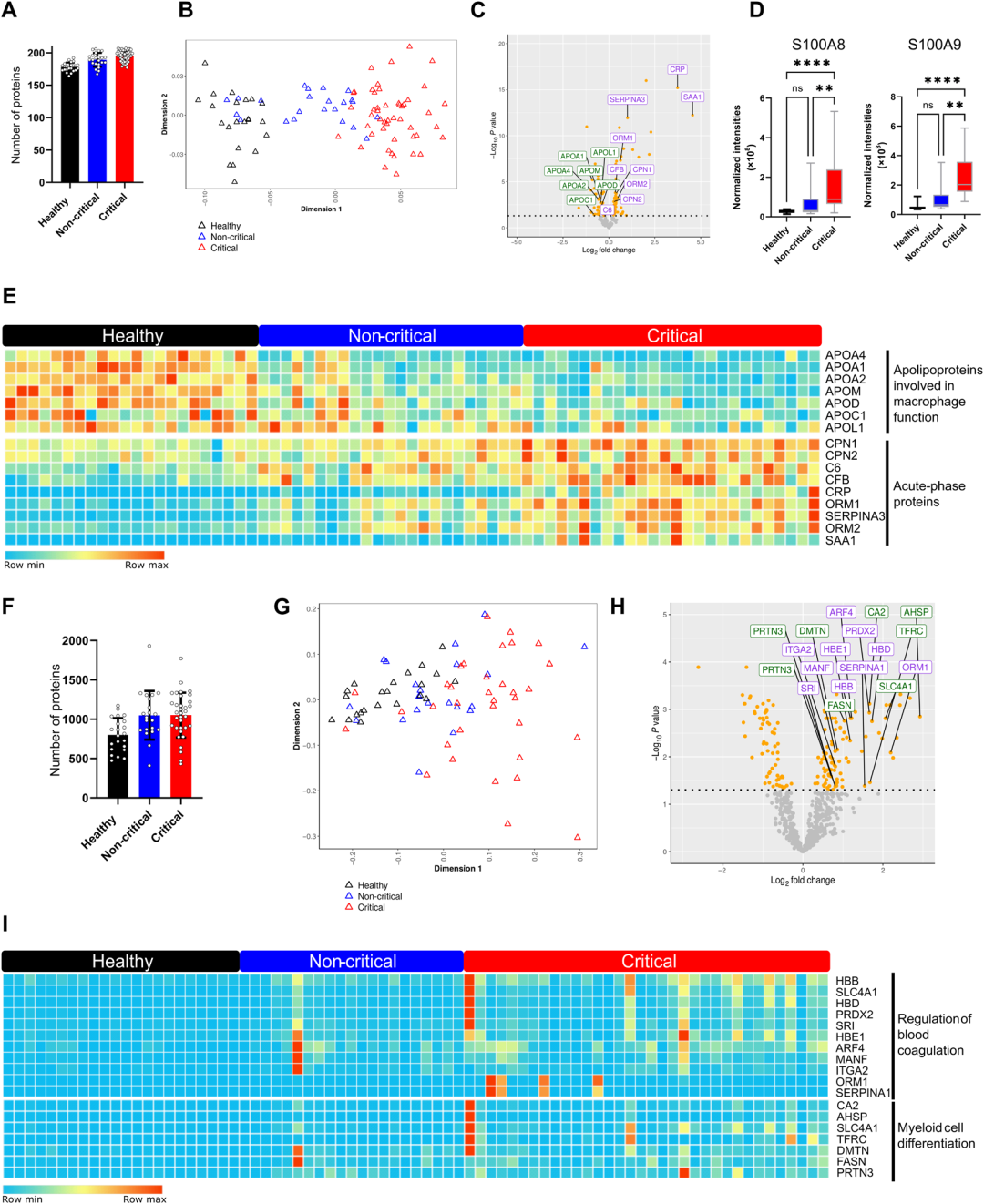
2. 血浆和PBMC蛋白质组学揭示了急性炎症、髓系激活和凝血失调的特征
研究者使用基于质谱的蛋白质组学对血浆样本中的蛋白进行检测(未去高丰度蛋白),共鉴定出336种蛋白质,其中健康个体、非危重患者和危重患者的平均检出蛋白数量分别为178±7个、189±11个和195个±8个。差异比较分析显示,与之前的研究一致,抗菌钙保护素(S100A8和S100A9的异源二聚体)是危重患者与非危重患者比较显著高表达的蛋白之一,这证实了钙保护素是疾病严重程度的可靠标记物。此外,差异比较还显示了多种载脂蛋白的失调,包括APOA1、APOA2、APOA4、APOM、APOD、APOC1和APOL1。这些蛋白大多数与巨噬细胞功能相关,并在危重患者中表达下调。急性期蛋白(CRP、CPN1、CPN2、C6、CFB、ORM1、ORM2、SERPINA3、SAA1)在危重症患者中表达强烈上调。这些发现与以往的研究结果一致,即急性炎症和过度的免疫细胞浸润与疾病的严重程度相关。
PBMC的蛋白质组学共鉴定和定量了2196个蛋白,其中健康对照组、非危重患者组和危重患者组的平均检出蛋白数量为801±213个、1050±309个和1052±286个。危重患者组和非危重患者组的差异表达分析显示了凝血和骨髓细胞分化失调。凝血蛋白包括血红蛋白亚基(HBB)、血红蛋白亚基(HBD)、血红蛋白亚基(HBE1)、SLC4A1、过氧化物还蛋白-2(PRDX2)、(SRI)、血基化因子4(ARF4)、中脑星形细胞源性神经营养因子(MANF)、整合素-2(ITGA2)、血红蛋白1(ORM1)和Serpin家族成员1(SERPINA1)的检测证实疾病的严重程度也与凝血相关并发症相关,可能涉及出血或血栓形成。
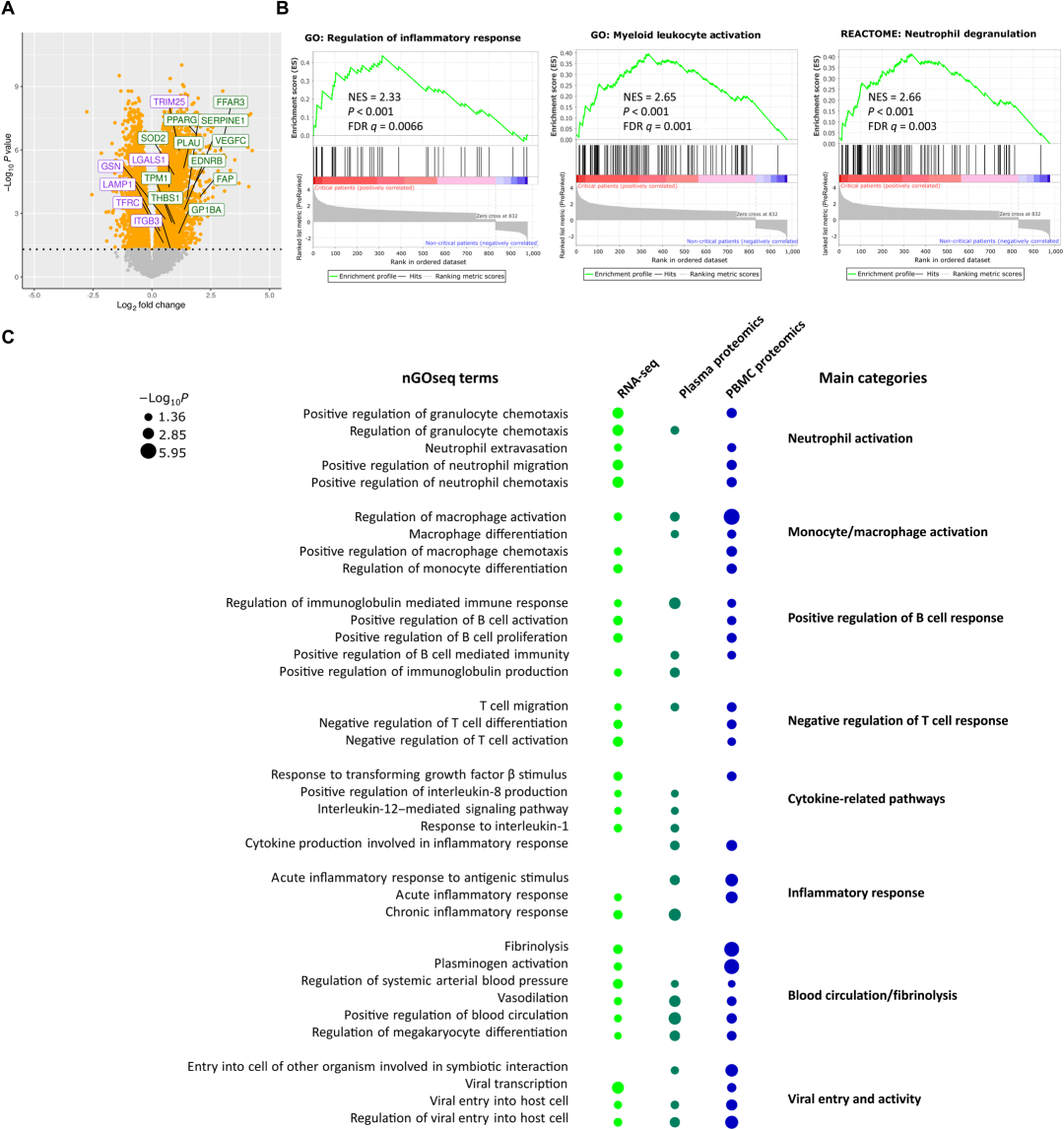
3. 转录组学和蛋白质组学联合分析确认危重疾病相关的炎症通路
与蛋白质组学数据一致,危重患者全血的RNA测序的结果显示了调节炎症反应、骨髓细胞活化和中性粒细胞脱颗粒等功能或通路的富集。全血RNA-seq、血浆及PBMC的蛋白质组学数据与细胞因子检测的结果一致,均强调了炎症信号通路和对促炎细胞因子释放(IL-1、IL-8和IL-12)的响应。此外,在三个组学数据集中,与病毒侵入甚至病毒转录相关条目在危重疾病患者中被强烈富集。这一结果与8例危重患者的RNA-seq数据中鉴定出的病毒基因转录本一致,但在非危重患者中却不一致。
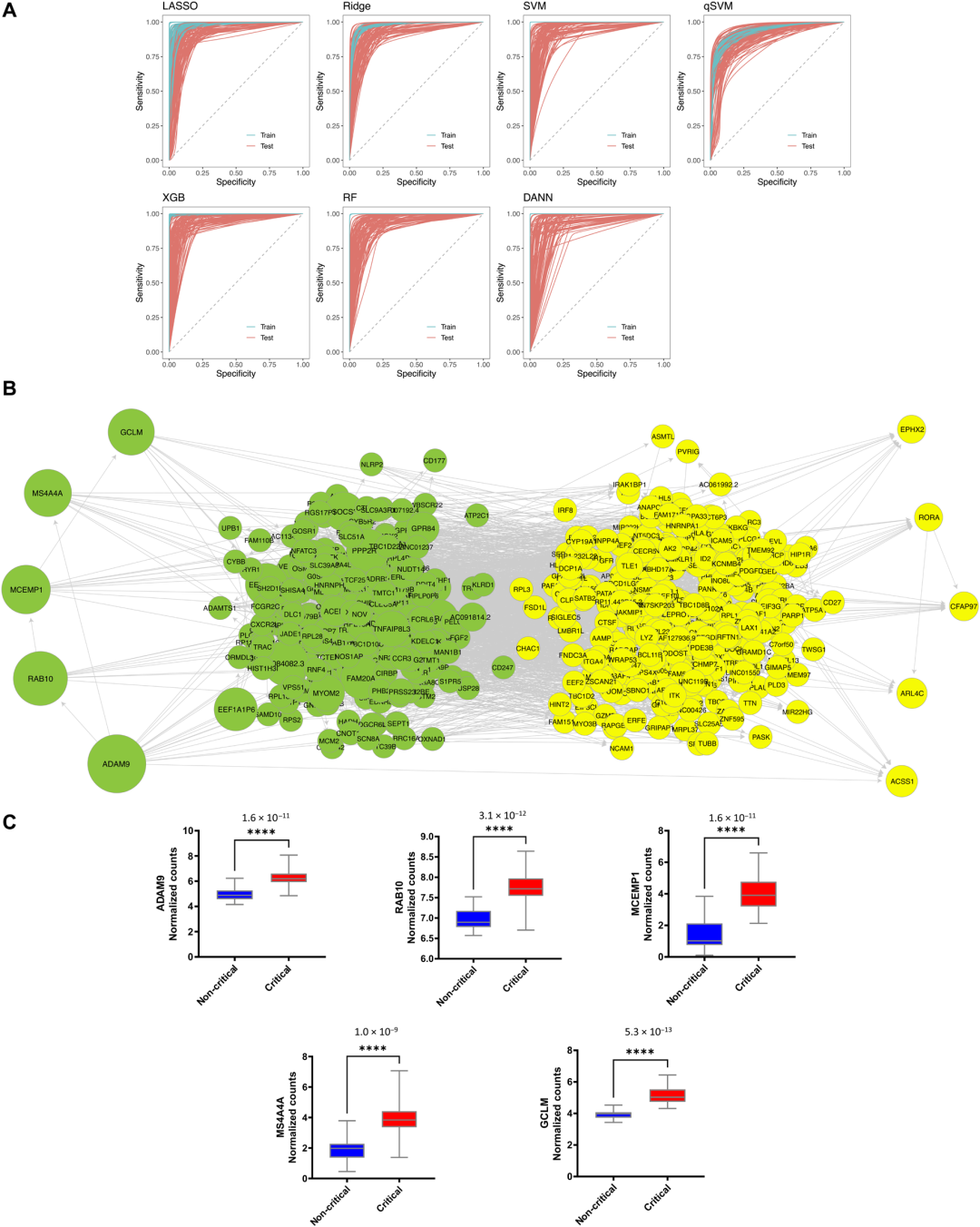
为了能稳健地识别可能区分非危重患者和危重患者的基因及可能与急性呼吸窘迫综合征(ARDS)进展相关的基因,研究者对69例患者的血液RNA-seq数据(46个危重和23个非危重患者)进行了100次计算。使用80%的样本用于训练,20%的样本用于测试,并评估7种不同的人工智能(AI)和机器学习(ML)算法的性能,包括量子支持向量机(qSVM),以区分非危重和危重COVID-19患者。经过不断的筛选,最终找了一组稳健和稳定的广泛特性基因。这一特征代表了数百个差异表达的基因,但它本身并不能区分危重COVID-19的驱动基因及对该疾病有响应的基因。因此,研究者选择了信息最丰富的前600个基因,并将它们作为结构因果建模(SCM)的输入基因,以确定关键COVID-19的可能驱动因素。通过仅使用这600个基因重新训练集成ML分类器,证实了这600个基因在区分危重和非危重患者方面具有生物学上的相关性。先前的研究表明,RNA-seq数据的SCM产生了因果依赖结构,这表明了细胞内发生的信号转导级联,并驱动表型和病理表型发育。前五个与假定的因果依赖程度最大的基因分别是ADAM9、RAB10、MCEMP1、MS4A4A和GCLM。
为了进一步评估上述筛选到的COVID-19基因表达特征的有效性,研究者使用了第二个独立的患者队列,包括COVID-19危重患者以及从ICU出院后3个月恢复的危重患者。驱动基因在第二个患者队列中遵循相同的趋势,即前述的5个基因在危重的COVID-19患者组中均显示出表达增加。此外,使用在前一个队列患者中识别出的600个基因在第二个队列上进行训练,最终得到的ML分类器能够很好地区分危重患者和康复患者。当对危重患者和康复患者之间的差异表达基因进行训练时的分类性能与第一个患者队列几乎相同,这进一步表明这一基因特征具有很大程度的生物学相关性。
5. ADAM9是COVID-19危重患者急性呼吸窘迫综合征(ARDS)的驱动因素
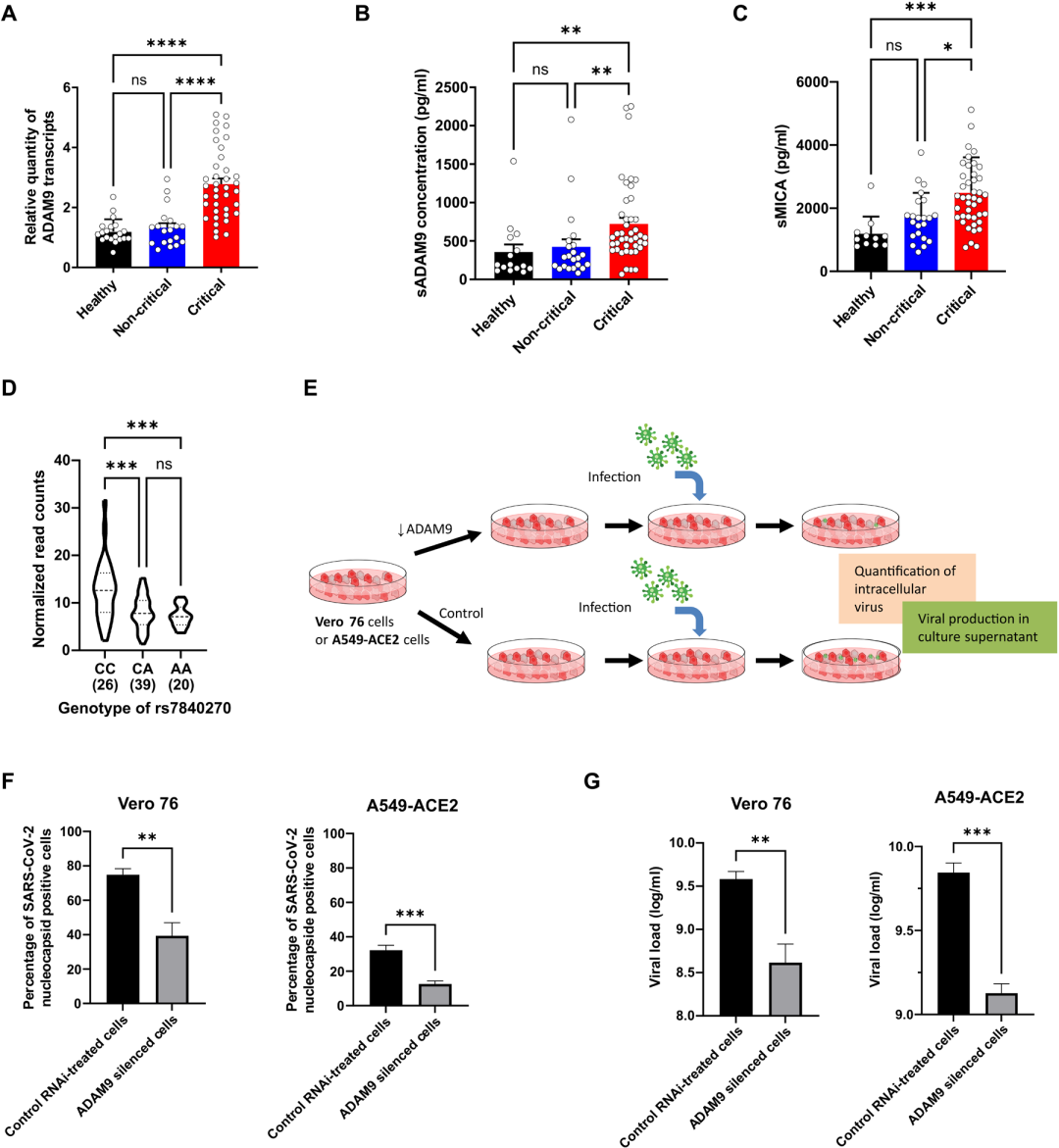
前述的五个驱动基因中,研究者挑选影响最显著的ADAM9(一种分解素和金属蛋白酶9)进行深入研究。ADAM9是一种具有多种功能的金属蛋白酶,可通过其分解素结构域粘附或通过其金属蛋白酶结构域介导大量细胞表面蛋白的脱落。ADAM9基因编码两种亚型,它们可以被翻译成膜结合蛋白或分泌蛋白。在危重患者与非危重患者血清中分泌型的浓度更高。此前的报道表明,ADAM9的转录上调与疾病的严重程度相关。为了评估危重队列中金属蛋白酶活性是否增加,研究者定量了已知能被ADAM9裂解的MICA蛋白。与非危重患者和健康对照组相比,危重患者血浆中可溶性MICA的浓度确实显著升高。
为了评估ADAM9在病毒感染中的作用,研究者建立了一种体外实验,在该实验中,通过siRNA在Vero76或A549-血管紧张素转换酶2(ACE2)细胞中沉默ADAM9,随后用SARS-CoV-2感染细胞。在这两种细胞系中,当ADAM9被沉默时,细胞内病毒的数量和释放的病毒的数量都较低。这些研究结果共同表明,ADAM9是危重患者体内上调的驱动因子。综合以上,研究者在危重患者的血清样本中检测到了更高的蛋白水解活性,并在体外细胞模型中证明了上调的ADAM9促进了病毒感染和复制。
研究结论
研究者通过对年轻的COVID-19危重患者、非危重患者及健康个体的多组学检测(全基因组测序、全血RNA测序、血浆和血液单个核细胞蛋白质组学、细胞因子谱分析和高通量免疫表型分析),并整合了机器学习、深度学习、量子退火和结构因果模型等算法,最终发现COVID-19危重患者的特征是炎症加重、淋巴系和髓系细胞腔区室紊乱、凝血功能增加和病毒细胞生物学特性增加。研究者还筛选到一个金属蛋白酶ADAM9的上调。该基因特征在81个危重患者和73个COVID-19康复患者的第二个独立队列中得到验证。体外ADAM9抑制降低了SARS-CoV-2在人肺上皮细胞中的摄取和复制。总之,研究者描绘了年轻的、其他方面都健康的COVID-19个体在新冠病毒感染后体内的生物学扰动,并发现一个基因特征集可以区分危重和非危重患者。此外,ADAM9是疾病严重程度的驱动因素和一个候选治疗靶点。
吉凯基因凭借多年在靶标筛选及验证服务领域的技术积累,建立的标准化 、工程化 、系统化的GRP平台,为中国研究型医生提供科研服务,加快科研成果转化。其中,多组学平台包含蛋白质组学平台和单细胞测序平台:
·蛋白质组学平台拥有多台timsTOF Pro、Exploris 480高精度质谱仪,专业的Spectronaut Plusar、Mascot等分析软件,提供专业的4D、DIA、TMT、PRM、磷酸化修饰组等检测服务,强大的机器学习算法、IPA分析、蛋白基因组分析服务,系统的生物标志物、分子分型、药物靶点、基因功能研究等解决方案,真正让广大研究型医生的科研工作更省心、更省力、更高效;
·单细胞测序拥有10x和BD两个平台,提供单细胞RNA-seq、单细胞核测序、单细胞混样RNA-seq、单细胞(RNA+ATAC)、空间转录组测序等服务。