上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
公司新闻/正文
国自然新宠——乳酸化修饰蛋白组在医学研究中的应用
709 人阅读发布时间:2025-06-03 17:19
乳酸(Lactate)是细胞糖酵解途径重要的含碳代谢产物,通常当细胞处于低氧环境下,葡萄糖通过“无氧糖酵解”途径产生乳酸。乳酸分泌是公认的癌症经典代谢特征——癌细胞即使在有氧条件下也倾向于利用糖酵解进行能量生产,导致乳酸产生增加,通常被称为Warburg效应[1]。
乳酸化修饰(Lactylation)于2019年由芝加哥大学赵英明教授领衔发现[2],通过乳酸与蛋白质的赖氨酸残基反应,形成乳酸化蛋白质。蛋白质乳酸化修饰是乳酸发挥功能的重要方式,乳酸化不仅限于组蛋白,还延伸到非组蛋白,从而影响多种细胞过程,包括调控细胞代谢和信号传导、在特定生理病理过程、肿瘤微环境、炎症微环境中发挥特定功能等。
近年来,乳酸化修饰(Lactylation)作为蛋白质翻译后修饰的新星,在生命科学领域掀起研究热潮。通过高通量蛋白组学技术,科学家们从海量文献中挖掘出乳酸化修饰的动态图谱,揭示了其如何通过调控线粒体功能、自噬通路和表观遗传机制影响疾病进程,从肿瘤微环境的代谢适应,到急性肾损伤中的线粒体失衡,乳酸化修饰蛋白组研究正为精准医学提供全新靶点。
案例一
MRE11乳酸化对同源重组修复的代谢调控

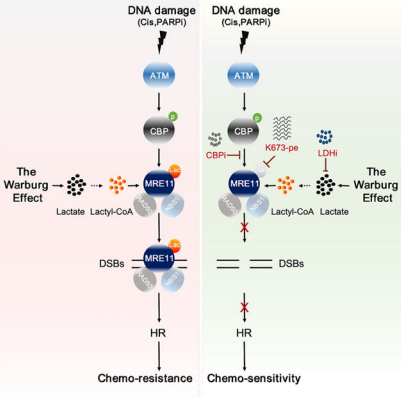
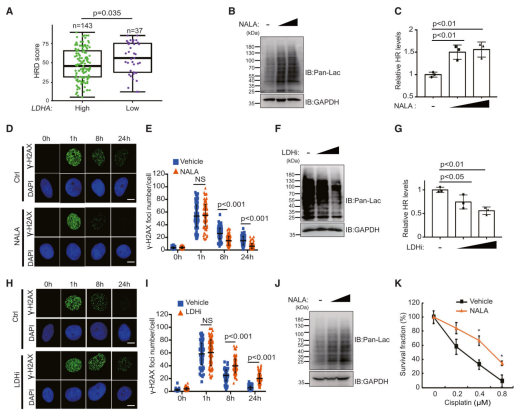
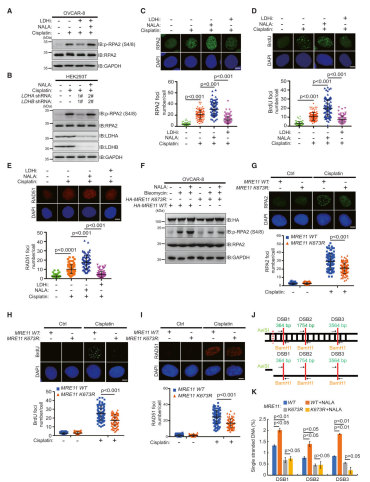
研究背景:同源重组(homologous recombination, HR)是双链DNA断裂(DSB)的高保真修复途径,依赖MRE11/MRN复合物启动DNA末端切除,在细胞增殖、癌症发生和癌症治疗中起着决定性作用。癌细胞通过Warburg效应产生大量乳酸,乳酸可诱导蛋白质乳酸化修饰。MRE11的功能受多种翻译后修饰调控(如磷酸化、泛素化),但乳酸化修饰尚未被报道。
研究目的:探究MRE11是否发生乳酸化修饰及其调控机制
研究对象:人细胞系(HEK293T、HCT116 结肠癌细胞、乳酸化缺陷MRE11 K673R 突变细胞)+动物模型(小鼠PDX模型、PDO类器官模型)
组学方法:乳酸化修饰组学+修饰泛抗体+位点特异性定制抗体
结论:MRE11的乳酸化修饰在同源重组(HR)中起关键作用。DNA损伤后,CBP乙酰转移酶在ATM磷酸化作用下催化MRE11的K673 位点乳酸化,增强其与DNA结合能力,促进DNA末端切除和HR修复。高乳酸环境通过提升 MRE11乳酸化水平导致肿瘤细胞化疗耐药。抑制CBP、LDH或使用特异性肽 K673-pe阻断MRE11乳酸化,可削弱HR修复并增强肿瘤对顺铂、PARPi的敏感性,为克服化疗耐药提供了新策略。
案例二
XRCC1乳酸化修饰促进胶质母细胞瘤的DNA损伤修复

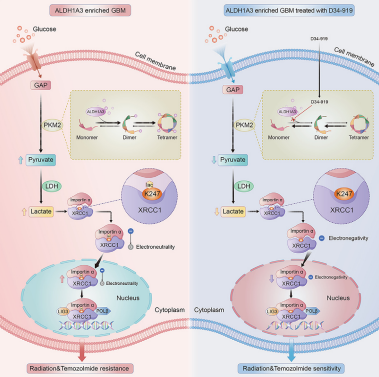
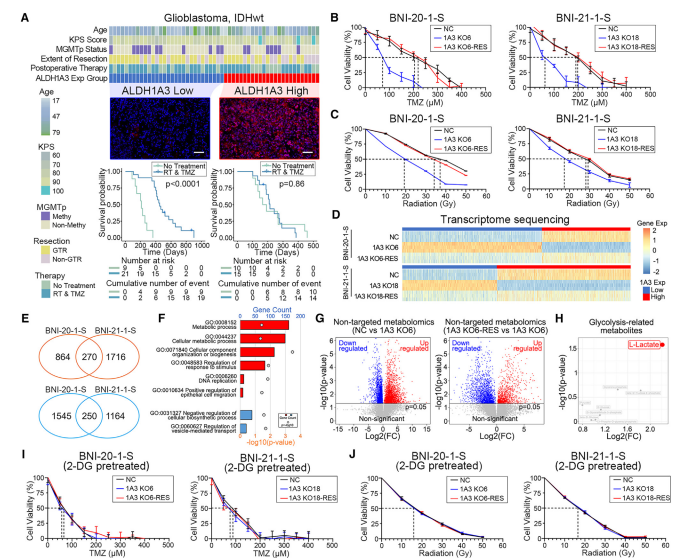
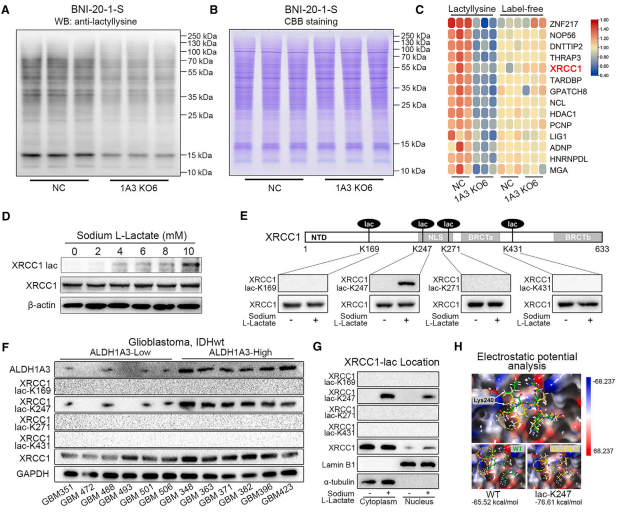
研究背景:胶质母细胞瘤(GBM)是最常见且侵袭性极强的原发性脑肿瘤,即使经过手术切除和术后放化疗,患者预后仍极差。ALDH1A3(醛脱氢酶1A3)的高表达与GBM患者对放化疗的抵抗及不良预后密切相关,但其具体机制尚未明确。糖代谢重编程和乳酸化修饰可能通过调控DNA修复功能参与肿瘤治疗抵抗,但二者在ALDH1A3介导的耐药中的作用仍不明确。
研究目的:探索ALDH1A3过表达如何通过糖代谢重编程诱导XRCC1乳酸化修饰
研究对象:细胞模型(ALDH1A3高表达的胶质母细胞瘤干细胞(GSCs)、患者来源的N33细胞系)+ 动物模型(小鼠颅内移植瘤模型及GBM类器官模型)
组学方法:乳酸化修饰组学+代谢组学
结论:胶质母细胞瘤(GBM)中ALDH1A3通过结合PKM2促进其四聚化,增加乳酸生成,导致XRCC1的K247位点乳酸化;乳酸化修饰改变XRCC1表面电荷,增强其与importin α的亲和力,促进核转位并提升DNA修复能力,从而介导放化疗抵抗。小分子化合物D34-919可特异性阻断ALDH1A3-PKM2相互作用,抑制PKM2四聚化及乳酸积累,逆转XRCC1乳酸化修饰,最终恢复GBM对放化疗的敏感性。D34-919在体内外模型中显著抑制肿瘤生长并延长生存期,为ALDH1A3高表达GBM患者提供了潜在治疗策略。
案例三
H3K18乳酸化通过YTHDF1/m6A/NREP途径促进砷相关特发性肺纤维化进展

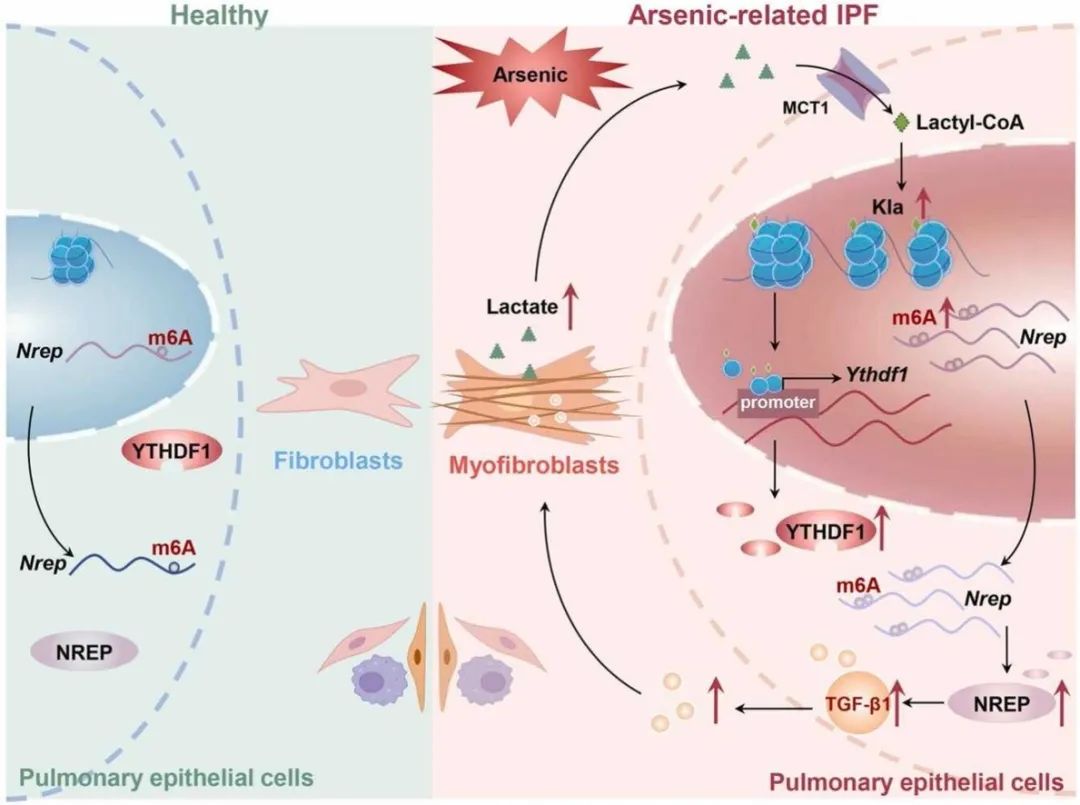
研究背景:长期暴露于砷(如饮用水污染)可增加特发性肺纤维化(IPF)风险,其特征包括肺泡上皮损伤、成纤维细胞向肌成纤维细胞转化(FMT)和细胞外基质沉积。乳酸进入细胞后转化为乳酰- CoA,在CBP/p300等酶催化下修饰组蛋白(如H3K1乳酸化,H3K18la)。mRNA的m6A甲基化由METTL3、FTO/ALKBH5和YTHDF1等蛋白调控,影响mRNA稳定性和翻译,与癌症和纤维化相关。H3K18la与m6A阅读器YTHDF1在砷诱导的肺纤维化(As-IPF)中的具体作用机制尚不明确。
研究目的:解析As-IPF中乳酸代谢、H3K18la 和 m6A 修饰的相互作用机制
研究对象:动物模型(C57BL/6J小鼠,对照组&砷暴露组)+细胞模型(肺泡上皮细胞、肌成纤维细胞、m6A 相关基因修饰细胞)
组学方法:乳酸化修饰组学+m6A meRIPseq +RNA-seq
结论:砷暴露诱导的特发性肺纤维化(As-IPF)中,肌成纤维细胞分泌的乳酸通过MCT1转运至肺泡上皮细胞(AECs),使组蛋白H3K18乳酸化(H3K18la)水平升高,促进m6A阅读器YTHDF1 转录;YTHDF1通过识别NREP mRNA 的 m6A 修饰位点,增强 NREP 蛋白表达并激活 TGF-β1 分泌,驱动成纤维细胞向肌成纤维细胞转化(FMT),加剧肺纤维化。研究揭示了 H3K18la-YTHDF1/m6A-NREP 通路在 As-IPF 中的关键作用,为靶向代谢 - 表观调控轴治疗肺纤维化提供了新方向。
案例四
组蛋白乳酸化增强ALKBH3表达并通过m1A去甲基化SP100A减少早幼粒细胞白血病蛋白核凝聚体,促进肿瘤进展

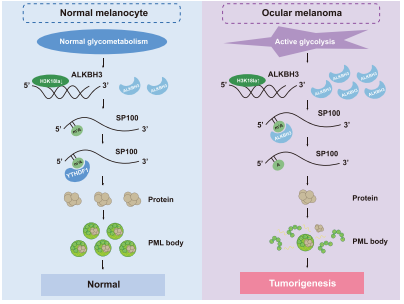
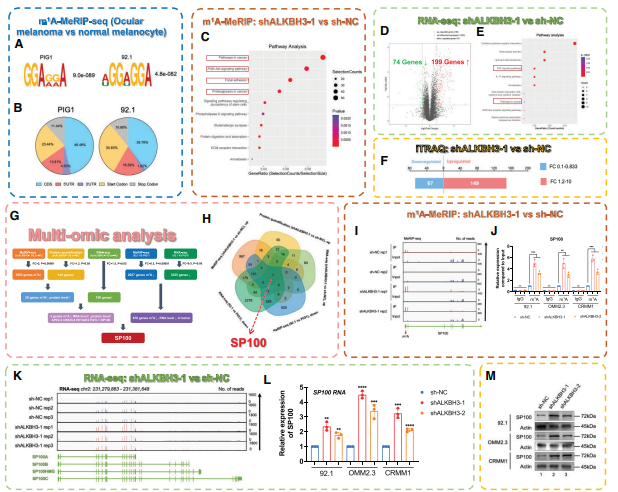
研究背景:眼黑色素瘤(包括葡萄膜黑色素瘤和结膜黑色素瘤)是最常见的眼内恶性肿瘤,具有化疗抵抗和高转移特性,其发病与表观遗传异常(如组蛋白修饰、m1A修饰)相关。前期研究发现,眼黑色素瘤中组蛋白乳酸化水平升高,但 m1A 修饰与乳酸化的互作机制未知。
研究目的:探索黑色素瘤中 m1A 修饰的动态变化及其与组蛋白乳酸化的关联
研究对象:临床样本(82 例眼黑色素瘤组织+28 例正常痣组织)+细胞模型(眼黑色素瘤细胞系+正常黑色素细胞系)+动物模型(裸鼠原位移植)
组学方法:乳酸化修饰组学+m1A meRIPseq+ RNA-seq
结论:组蛋白乳酸化通过上调 ALKBH3 表达,促进 SP100A 的 m1A 去甲基化,降低其 RNA 稳定性和翻译效率,减少 PML 核凝聚体形成,从而推动眼黑色素瘤进展。机制上,H3K18 乳酸化富集于 ALKBH3 启动子,驱动其转录,而 ALKBH3 通过去除 SP100A 的 m1A 修饰(如 c.A92 位点)抑制其功能。敲低 ALKBH3 或过表达 SP100A 可抑制肿瘤生长,揭示了“乳酸化 - ALKBH3-m1A-SP100A-PML” 通路在肿瘤中的关键作用,为靶向 m1A 重编程治疗提供了新方向。ALKBH3在高风险眼黑色素瘤中因组蛋白乳酸化水平过高而特异上调,表现为m1A低甲基化状态。
案例五
单细胞转录组分析揭示组蛋白乳酸化与膀胱癌顺铂耐药的相关性

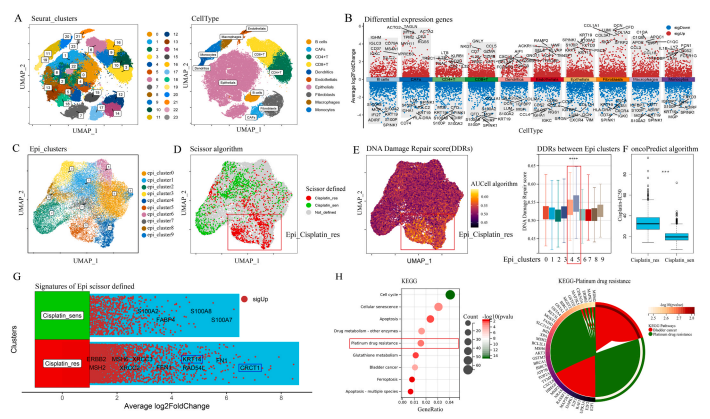
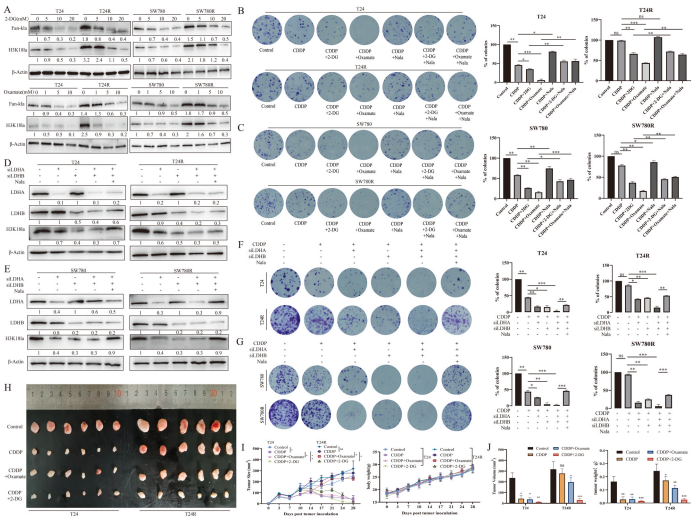
研究背景:膀胱癌(BCa)是全球第十大常见恶性肿瘤,顺铂(Cisplatin)是治疗晚期膀胱癌的主要化疗药物,但约65%患者最终会产生耐药性,导致治疗失败。目前已知的耐药机制包括药物外排增强、DNA损伤修复异常等,但单一靶向策略效果有限。近年研究发现,表观遗传调控(如组蛋白修饰)在耐药中起关键作用。乳酸化修饰(Lactylation)作为一种新型翻译后修饰,与肿瘤代谢重编程密切相关,但其在顺铂耐药中的作用尚不明确。
研究目的:通过单细胞测序及修饰蛋白组学揭示膀胱癌顺铂耐药的分子机制,探索组蛋白乳酸化修饰(如H3K18la)对耐药性形成的调控作用
研究对象:临床样本(GEO数据库的膀胱癌单细胞转录组数据,含顺铂耐药与敏感样本)+细胞模型(顺铂耐药膀胱癌细胞系)+动物模型(顺铂耐药细胞移植的裸鼠皮下瘤模型)
组学方法:单细胞测序+乳酸化修饰组学
结论:膀胱癌中存在特定的顺铂耐药上皮细胞亚群,其特征为高糖酵解活性、鳞状分化标记物高表达及肿瘤微环境中异常细胞通讯。乳酸积累导致组蛋白H3K18la水平显著升高,并通过富集于YY1/YBX1启动子激活其转录,进而调控DNA 损伤修复、EMT 及细胞凋亡抵抗等通路,促进耐药性。H3K18la、YBX1和YY1可作为克服顺铂耐药的关键干预靶点。
案例六
在急性肾损伤(AKI)中,ALDH2的乳酸化加剧了线粒体功能障碍并通过破坏PHB2介导的线粒体自噬发挥作用

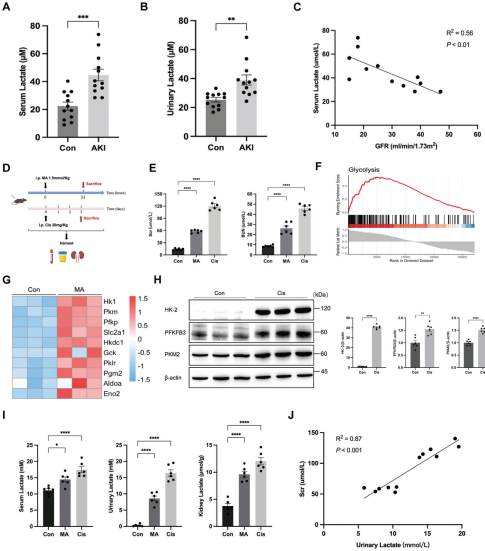
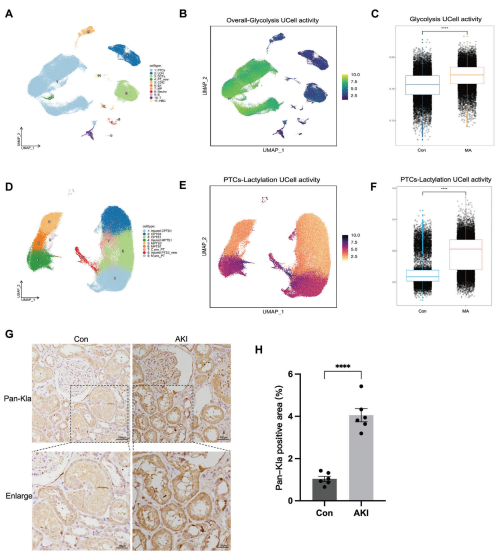
研究背景:近端小管细胞(PTCs)线粒体密度高,易受损伤,线粒体数量减少、结构变形及膜电位下降是急性肾损伤(AKI)的关键病理特征。线粒体功能障碍导致糖酵解增强、乳酸积累,乳酸水平与AKI患者肾小球滤过率(GFR)呈负相关。
研究目的:探究AKI中乳酸水平与乳酸化修饰的关联及ALDH2 乳酸化影响线粒体自噬的分子机制
研究对象:临床样本(AKI 患者与对照的血清、尿液及肾活检组织)+动物模型(C57BL/6 小鼠)+细胞模型(人近端小管细胞 HK-2)
组学方法:乳酸化修饰+单细胞测序(scRNAseq)
结论:AKI 患者及小鼠肾组织中乳酸水平与乳酸化修饰(pan-Kla)显著升高,ALDH2在K52位点的乳酸化抑制其酶活性,导致线粒体功能障碍和肾小管损伤。ALDH2乳酸化通过促进PHB2的泛素化-蛋白酶体降解,抑制线粒体自噬,从而加重线粒体损伤。SIRT3作为去乳酸化酶,可通过降低ALDH2乳酸化水平恢复PHB2稳定性,改善线粒体自噬和肾功能。靶向ALDH2乳酸化或激活SIRT3可能成为AKI的新型治疗策略。
吉凯基因现已开展包括乳酸化等多种修饰蛋白组服务,想了解更多详情,请咨询当地销售经理。
【参考文献】
1. Warburg, O, 2019. On the origin of cancer cells. Science.
2. Zhang,D., et al., 2019. Metabolic regulation of gene expression by histone lactylation. Nature.