上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
公司新闻/正文
干货!单细胞测序视角下的胎盘研究文献专题
1258 人阅读发布时间:2025-07-02 10:42
胎盘(placenta)由滋养层细胞发育而来,是维系妊娠成功的关键器官,它不仅构成了母体与胎儿之间的屏障,更承担着氧气、营养物质和代谢废物交换等多重功能。在妊娠过程中,滋养层细胞会分化为细胞滋养层细胞(cytotrophoblast, CTB)、绒毛外滋养层细胞(extravillous trophoblast cells, EVT)和合体滋养层细胞(syncytiotrophoblast, STB)等多种细胞类型。单细胞测序可以帮助我们细致地探索胎盘细胞类型的特异性功能和相互作用,以及它们如何在不同的妊娠阶段及妊娠并发症中变化,进而更精确地定义胎盘细胞的分子特征,帮助我们理解复杂的胎盘生物学和其在母胎健康中的关键作用。
案例一
单细胞RNA测序识别CXADR为胎盘交换面的命运决定因素

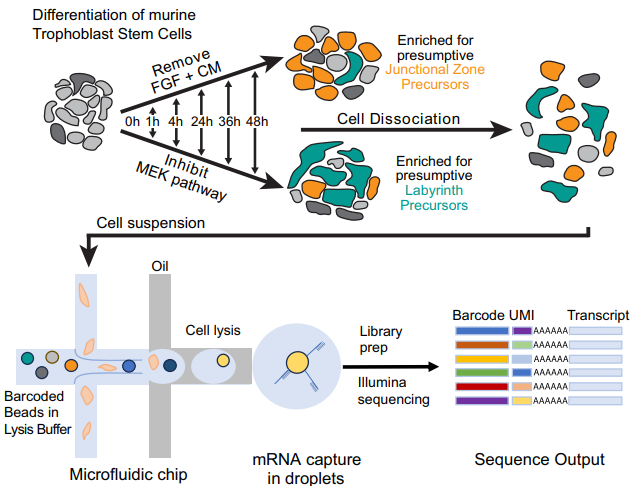
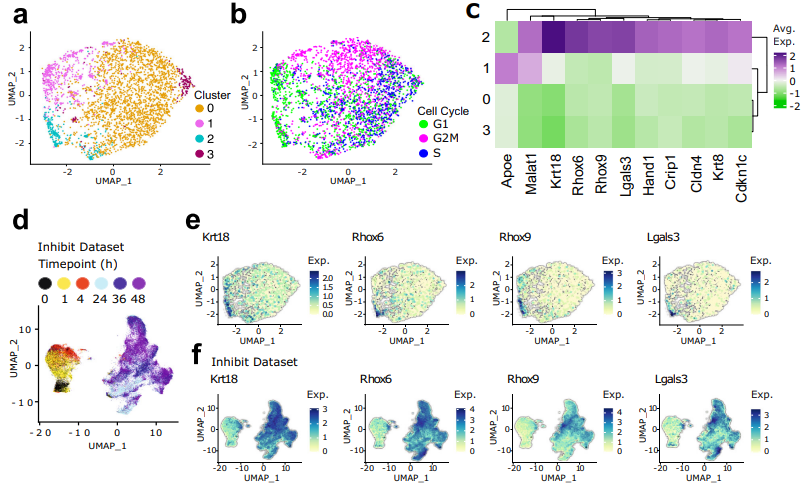
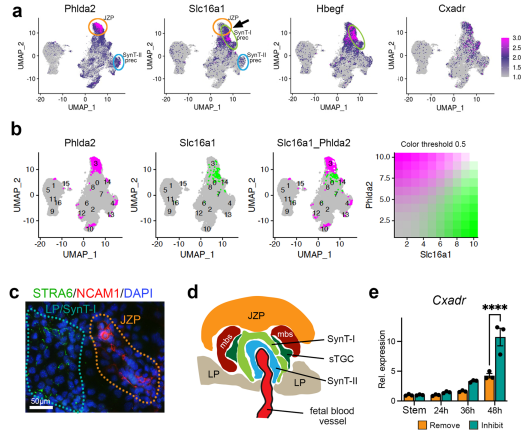
研究背景:胎盘是母胎之间的关键界面,它不仅构成了母体与胎儿之间的屏障,更承担着氧气、营养物质和代谢废物交换等多重功能。胎盘功能障碍是许多妊娠并发症(如子痫前期、胎儿生长受限等)的基础。胎盘发育过程需要滋养层干细胞(trophoblast stem cells, TSCs)的适当扩张和精确的谱系分化,但相关分子机制仍不明确。
研究目的:利用单细胞RNA测序揭示驱动胎盘滋养层干细胞(trophoblast stem cells, TSCs)命运偏向并决定SynT-I与SynT-II分化路径的关键调控因子。
样本信息:小鼠细胞系(源自早期小鼠囊胚的滋养外胚层)
组学策略:单细胞测序(Drop-seq)
捕获细胞数:136,291个
结论:通过对小鼠滋养层干细胞在分化早期阶段进行单细胞RNA测序,识别出干细胞状态的调控因子,特别是Nicol1,揭示了细胞谱系分化中未预料到的轨迹以及谱系进入点的调控因子。对其中一个谱系前体标志物CXADR的功能分析表明,这种细胞表面蛋白不仅是SynT前体细胞的标志物,更是调控SynT-I/SynT-II命运平衡的关键因子。其表达的时空精准调控对于维持胎盘交换面的功能完整性至关重要。解码滋养层谱系指定的机制将有助于我们理解人类妊娠在健康和疾病中的机制。
案例二
小鼠胎盘时空转录图谱

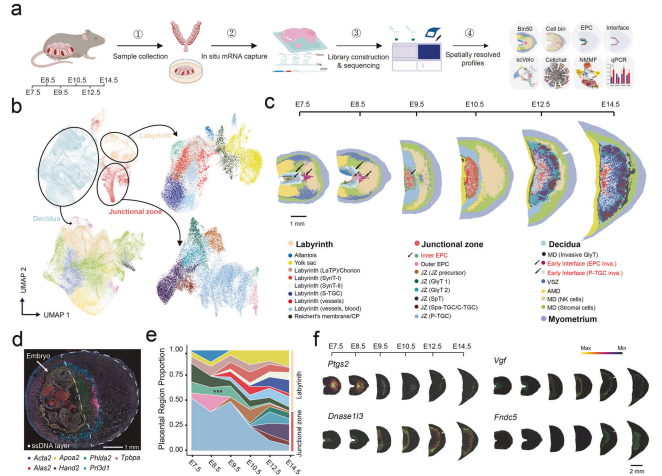
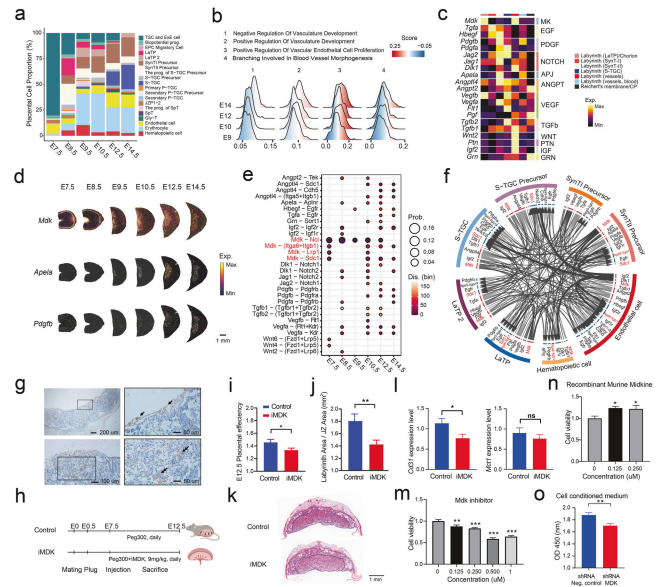
研究背景:胎盘是妊娠期间母胎营养交换的关键器官,其发育异常与多种妊娠并发症(如子痫前期、胎儿生长受限)相关。然而,胎盘发育过程中基因表达的时空模式仍缺乏系统解析。
研究目的:通过空间转录组测序结合单细胞RNAseq揭示包含多核合体滋养层细胞和多倍体滋养层巨细胞的胎盘细胞空间定位和基因空间表达模式。
样本信息:小鼠13个发育阶段的子宫切片(含胚胎、胎盘、蜕膜)。
组学策略:空间转录组测序(Stereo-seq)+ scRNA-seq (小鼠胎盘已发表数据)。
捕获细胞数:NA
结论:通过空间转录组结合单细胞数据构建了覆盖胚胎期(E)7.5至E14.5的小鼠胎盘时空转录组图谱,定义了外胎盘锥(早期异质性滋养外胚层结构)的四个不同层级,并阐明了E9.5前植入后早期阶段滋养层分化的空间轨迹。聚焦于小鼠胎盘营养交换界面的迷路区,揭示了对滋养层发育和胎盘血管生成至关重要的关键调节因子。合体滋养层细胞可能通过分泌Midkine调节胎盘血管内皮细胞的发育。父源表达基因特异性富集于胎盘而非蜕膜区域,可能参与胎盘血管生成的基因。在滋养层侵袭界面,鉴定出参与妊娠维持的界面特异性转录因子调控网络,如Atf3、Jun、Junb、Stat6、Mxd1、Maff、Fos和Irf7。此外,研究显示母体高脂饮食暴露优先影响该界面,加剧炎症反应并破坏血管生成稳态。研究为未来探索胎盘形态发生和病理机制提供了数据资源。
案例三
单细胞RNA测序揭示了胎盘在环境压力下的响应机制

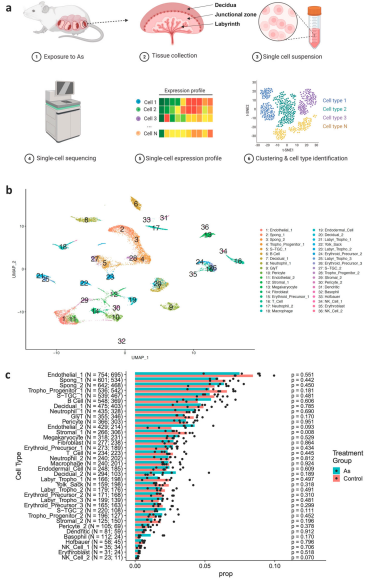
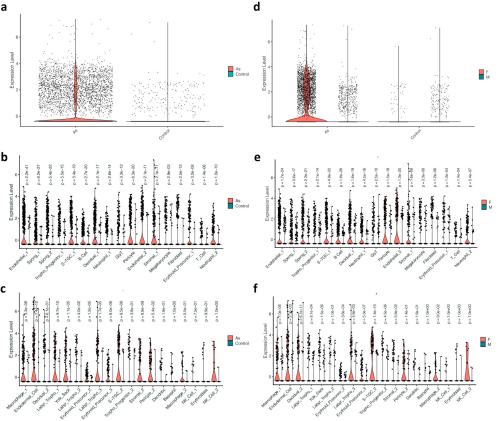
研究背景:胎盘是胎儿发育的关键器官,参与营养交换、激素分泌等多种功能。砷作为一种常见的环境毒物,其暴露与妊娠并发症(如早产、胎儿生长受限)和儿童神经发育缺陷相关,但胎盘对砷暴露的分子反应机制尚不明确。
研究目的:利用scRNA-seq识别砷暴露下小鼠胎盘的细胞类型特异性基因表达变化。
样本信息:坤暴露后的小鼠E17.5胎盘(含蜕膜)
组学策略:scRNA-seq(10x Genomics)
捕获细胞数:36,000个
结论:砷暴露诱导小鼠胎盘26种细胞类型特异性转录组变化,核心基因PRAP1在26种细胞类型(尤其是滋养层细胞)中显著上调,且雌性胎盘中PRAP1表达增幅高于雄性。免疫荧光显示PRAP1蛋白富集于胎盘交界区,可能通过调控分泌功能及内质网应激响应抵抗砷毒性。体外实验证实,重组 PRAP1 蛋白可降低砷诱导的人滋养层细胞毒性,下调细胞周期相关基因(如CDKN1A、CCNE1),通过抑制细胞周期(G2/M阻滞)和凋亡通路发挥保护作用。性别差异分析表明,雌性胎盘及人iPSC分化的滋养层细胞中PRAP1上调更显著,可能与雌激素信号或X染色体剂量效应相关。砷暴露导致脂代谢紊乱、炎症激活及蛋白质稳态失衡,而PRAP1可能通过调控这些通路维持胎盘功能。该研究为环境毒物致妊娠并发症的性别差异机制提供了新见解,并提示PRAP1作为潜在干预靶点的临床价值。
案例四
妊娠早期母体感染 SARS-CoV-2 后母胎界面的免疫再平衡

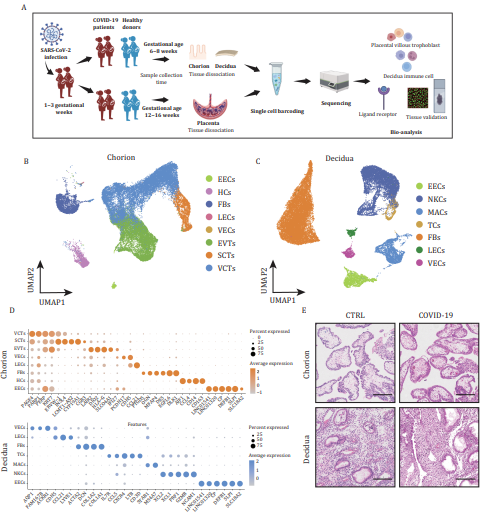
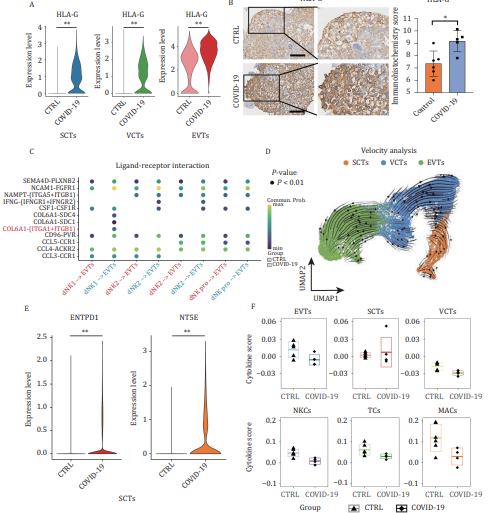
研究背景:已有研究表明,孕期感染SARS-CoV-2与胎儿并发症相关。孕早期是胎盘发育和器官发生的关键时期,此时母体感染对母胎界面的影响尚不明确。
研究目的:利用scRNA-seq探究SARS-CoV-2感染对母胎界面的影响
样本信息:34名孕妇的胎盘样本(包括绒毛膜、蜕膜(孕早期)和胎盘组织(孕中期)
组学策略:scRNA-seq(华大DNBelab C)+代谢组
捕获细胞数:84,331个
结论:SARS-CoV-2感染在孕早期母胎界面引发广泛的抗病毒反应,并诱导了氨基酸和磷脂谱的代谢改变,免疫细胞(如T细胞、自然杀伤细胞、巨噬细胞)和胎盘绒毛滋养层细胞均参与其中,同时滋养层细胞的免疫耐受性增强。随着胎盘发育,SARS-CoV-2感染对母胎界面的影响逐渐减弱,免疫细胞和滋养层细胞的变化趋于正常,代谢变化也逐渐恢复,表明胎盘在发育过程中能够适应病毒感染带来的影响,形成新的动态平衡。
案例五
妊娠早期人类子宫自然杀伤细胞调节绒毛外滋养细胞分化

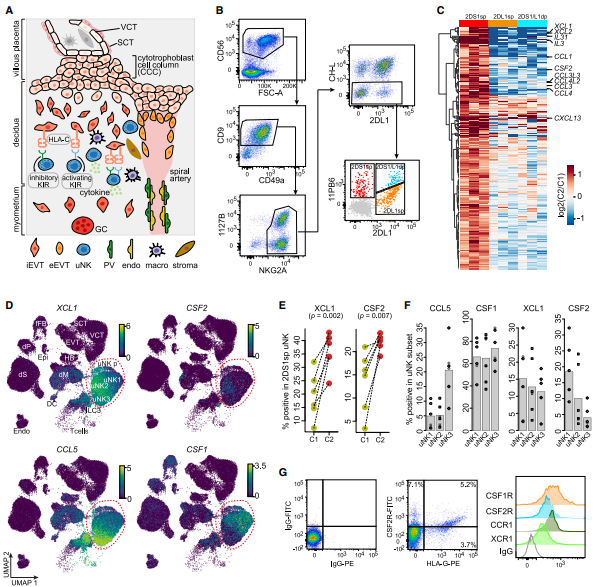
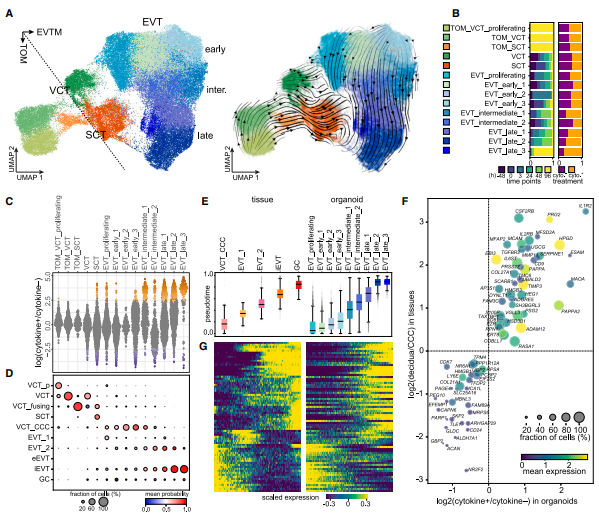
研究背景:在人类妊娠早期,绒毛外滋养层细胞(extravillous trophoblast cells,EVTs)侵袭子宫蜕膜,并重塑母体螺旋动脉,对于成功妊娠至关重要。尽管已有证据表明子宫自然杀伤细胞(uterine natural killer cells,uNKs)参与调控这一过程,但其具体的分子机制仍不明确。
研究目的:通过单细胞测序探究子宫自然杀伤细胞如何影响胎盘形成。
样本信息:人胎盘滋养层类器官
组学策略:scRNA-seq(10x Genomics)+蛋白组
捕获细胞数:67,996个
结论:研究结合人类胎盘类器官模型和原代组织样本,发现了四种uNK特异性的细胞因子(XCL1, CSF2, CSF1和CCL5),通过调节相关基因信号通路,增加分化程度更高EVTs的丰度和调节上皮-间质转化、细胞侵袭和细胞融合,从而对EVT分化起促进作用。这些信号还影响参与调节血流、营养物质、炎症和适应性免疫反应的转录程序,以及与子痫前期等妊娠疾病相关的基因特征。研究结果揭示了 uNK 细胞与滋养层之间最佳免疫相互作用如何增强生殖成功的机制。
案例六
通过单细胞RNA测序解析胎盘在分娩过程中的母胎相互作用

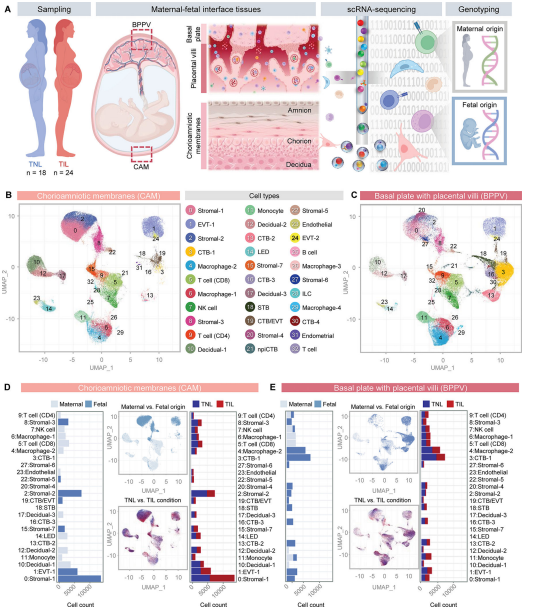
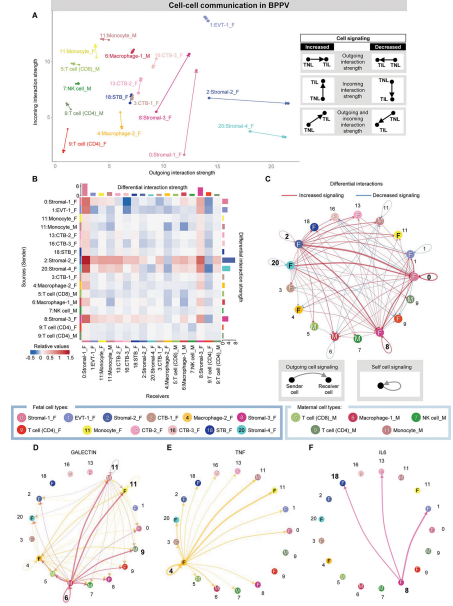
研究背景:分娩涉及母亲和胎儿生理、生化、内分泌和免疫等多系统的协调激活,但母胎间细胞通讯和相互作用机制尚未完全明确。此前研究虽对妊娠各阶段胎盘细胞组成有所了解,但缺乏对分娩时母胎界面全面的单细胞层面研究。
研究目的:通过单细胞测序探索分娩过程中母体和胎儿之间的细胞相互作用
样本信息:足月分娩妇女的胎盘及胎盘外组织样本
组学策略:scRNA-seq
捕获细胞数:NA
结论:母体和胎儿细胞类型在分娩过程中发生了转录组活性的变化,与胎盘组织相比,胎盘外组织绒毛膜羊膜(chorioamniotic membranes, CAMs)显示出更多与分娩高度相关的细胞类型,其中,受分娩影响最显著的细胞群是胎儿间质细胞、母体蜕细胞和母体巨噬细胞。CAM和胎盘细胞类型参与分娩驱动的母-胎信号传导,包括胶原蛋白、C-X-C基序配体(CXCL)、肿瘤坏死因子(TNF)、半乳糖凝集素和白细胞介素-6(IL-6)通路。这些信号通路主要涉及免疫细胞和非免疫细胞之间相互作用,进而影响炎症通路。
案例七
人胎盘合体滋养层细胞的单核多组学分析揭示了妊娠期间的细胞发育轨迹

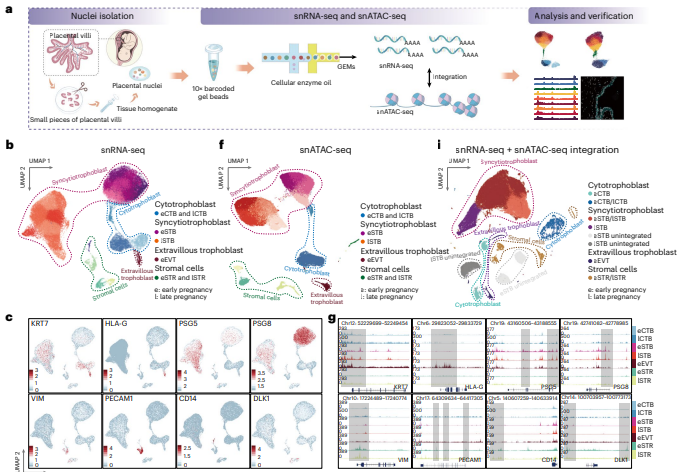
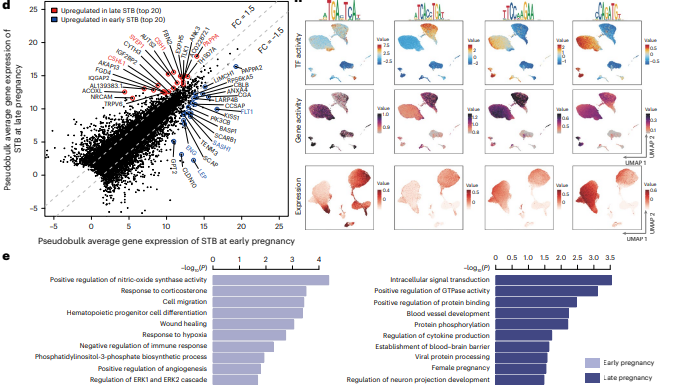
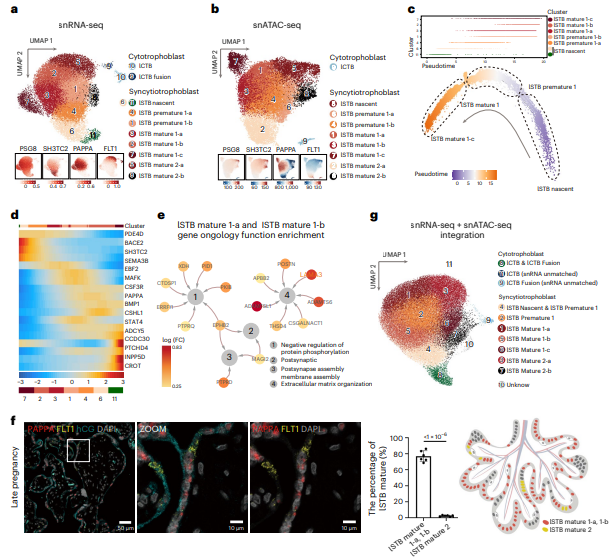
研究背景:胎盘是母胎界面的关键器官,负责营养供应、废物清除等功能。合体滋养层(nuclei within the syncytiotrophoblast, STB)作为胎盘的主要功能单元,是直接接触母体组织和血液的多核细胞,在激素合成、免疫防御等方面起关键作用。既往组织学研究提示核亚群存在,但STB核的转录和功能动态变化缺乏系统解析。
研究目的:通过整合snRNA-seq和snATAC-seq,构建早晚期妊娠STB核的单细胞图谱,明确核亚群的转录和表观特征
样本信息:12例健康胎盘(6例早期妊娠+6例晚期妊娠)
组学策略:单细胞核测序(snRNA-seq)+单细胞染色质可及性测序(snATACseq)
捕获细胞数:50,850个(snRNA-seq)+50,693 个(snATACseq)
结论:通过对早期和晚期妊娠的人类胎盘进行整合单细胞核 RNA 测序和单细胞核ATAC测序分析发现,早期妊娠中STB 核分为6个亚群,从新生态(eSTB nascent,SH3TC2+)到成熟态(eSTB mature1/2,PAPPA+或FLT1+),轨迹呈分叉状,分别关联生长激素信号和氧响应功能。晚期妊娠中,STB 核以成熟1型(lSTB mature 1,PAPPA+)为主,FLT1+核减少,染色质可及性动态与功能转变一致。通过基因调控网络鉴定了与多种 STB 核谱系相关的转录因子,如MITF和 STAT5A驱动eSTB mature 1分化(调控 PAPPA、CSH2),CEBPB和FOSL2调控eSTB mature 2(调控 FLT1),HIF1A参与早期低氧响应等。STB核异质性相关基因(如 FLT1、CEBPB)与子痫前期中绒毛外滋养层细胞( extravillous trophoblast cells, EVT)功能异常关联,为妊娠并发症的分子机制和生物标志物开发提供依据。