上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
公司新闻/正文
单细胞技术揭示PTSD的分子机制——创伤后应激障碍的“细胞密码”被破解
442 人阅读发布时间:2025-07-18 12:34
PTSD——看不见的伤痕
创伤后应激障碍(PTSD)是一种由极端创伤事件引发的复杂精神疾病,患者常经历闪回、情绪麻木和过度警觉等症状。全球约6%-8%的人口受其困扰,而军人、急救人员等高危群体的发病率更高。尽管PTSD与遗传、环境因素密切相关,但其分子机制长期未明。近日,一项发表于《Nature》的重磅研究通过单细胞多组学技术,首次在细胞层面揭示了PTSD患者前额叶皮层的基因表达和表观遗传变化,为理解这一疾病的生物学基础提供了全新视角。

研究概况:200万细胞解码PTSD
这项由耶鲁大学、加州大学欧文分校等机构合作的研究,分析了111例人脑样本(36例PTSD、36例抑郁症(MDD)和39例健康对照),覆盖超过200万个细胞核的单细胞转录组(snRNA-seq)、染色质可及性(snATAC-seq)和空间转录组数据。研究聚焦于大脑背外侧前额叶皮层(DLPFC)——一个与情绪调节和记忆整合相关的关键脑区,通过多模态分析揭示了PTSD特异的细胞类型变化和分子通路异常。
关键发现:PTSD的“细胞地图”
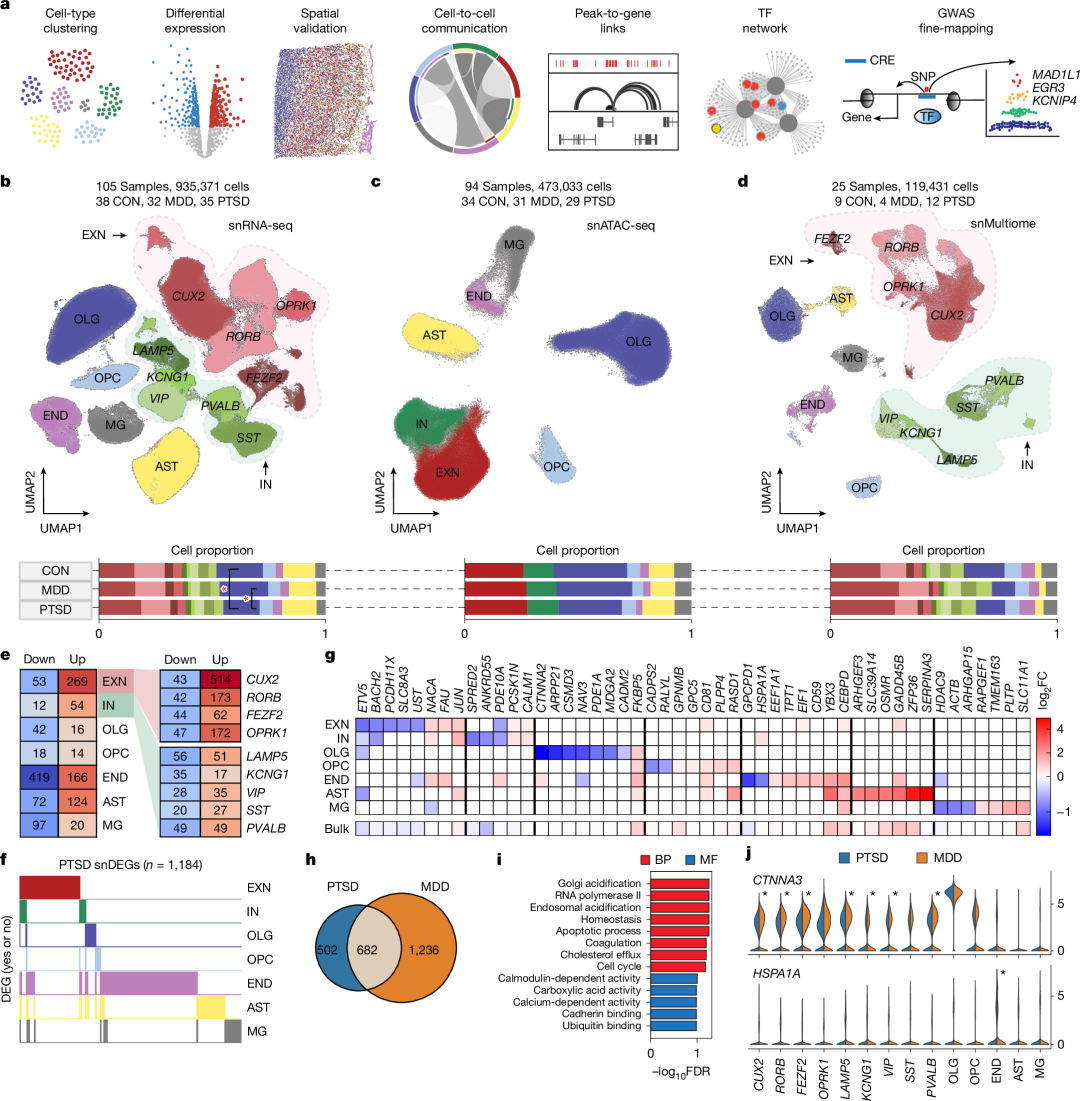
1 细胞类型特异性差异
o 抑制性神经元(SST interneurons):SST中间神经元(分泌生长抑素)的突触输出显著降低,导致GABA能信号传导减弱,可能解释PTSD患者的情绪调节障碍。
o 内皮细胞(Endothelial cells):与应激相关的基因(如FKBP5)在内皮细胞中异常高表达,提示血脑屏障功能可能参与PTSD的病理过程。
o 小胶质细胞(Microglia):与抑郁症不同,PTSD患者的小胶质细胞神经炎症信号(如SPP1通路)活性降低,表明两种疾病可能存在相反的免疫调控机制。
2与抑郁症的异同
o 57.6%的差异表达基因(DEGs)在PTSD和MDD中重叠,但PTSD特有基因富集于钙信号(如CALM1)、细胞黏附(如CTNNA3)等通路。
o 关键基因HSPA1A在内皮细胞中“PTSD下调、MDD上调”,提示二者在应激反应中的分化机制。
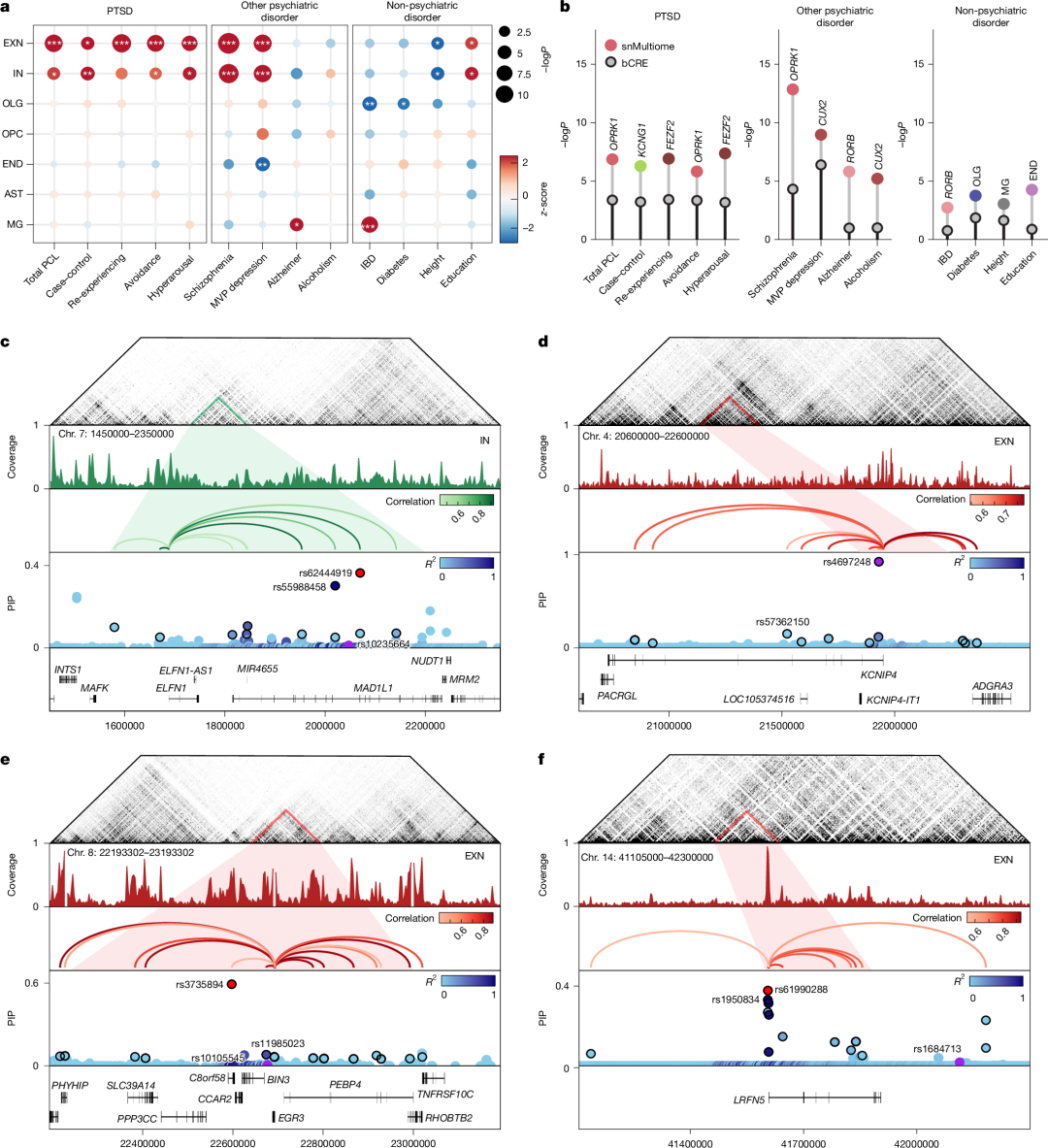
3 遗传风险位点的细胞特异性调控
o 通过精细定位(fine-mapping),研究发现了8个PTSD风险基因(如ELFN1、KCNIP4)的细胞类型特异性调控元件,其中ELFN1-MAD1L1位点的染色质环可能通过影响抑制性神经元突触功能增加患病风险。
技术亮点:多组学整合的典范
1.单细胞分辨率:结合snRNA-seq和snATAC-seq,首次在PTSD中构建了细胞类型特异的基因调控网络(如EGR2转录因子在兴奋性神经元中的调控作用)。
2.空间验证:通过Xenium空间转录组技术,在组织原位确认了FKBP5在内皮细胞中的高表达及SST神经元的空间分布异常。
3.跨物种验证:在小鼠创伤应激模型(SPS)中,证实了SST神经元到兴奋性神经元的突触传递减弱,与人类数据高度一致。
临床意义:从机制到治疗
这项研究不仅揭示了PTSD的细胞和分子靶点(如SST神经元、FKBP5通路),还为开发精准疗法提供了方向:
o 靶向GABA能系统:增强SST神经元活性或GABA受体功能(如GABRA5)可能改善症状。
o 调控内皮细胞应激反应:FKBP5抑制剂或成为潜在干预手段。
o 诊断标志物:血液中FKBP5或炎症因子的水平可能辅助PTSD的早期筛查。
结语:照亮PTSD的黑暗迷宫
论文通讯作者Matthew Girgenti博士表示:“这项研究像一盏探照灯,照亮了PTSD复杂的细胞和分子迷宫。”未来,结合类器官模型和药物筛选,这些发现有望加速抗PTSD药物的开发,为患者带来新的希望。