上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
公司新闻/正文
Adv Sci:转录组+蛋白质组揭示间充质干细胞来源的凋亡小泡靶向调控CD8+ T细胞稳态缓解超敏反应的作用机制
422 人阅读发布时间:2025-07-24 10:36

凋亡是维持多细胞生物稳态的重要过程。间充质干细胞(mesenchymal stem/ strom cells, MSCs)来源的凋亡囊泡Apoptotic vesicles(MSCs-ApoVs)作为天然脂质纳米颗粒,继承了亲本细胞的特性,在免疫治疗中具有潜力,但在CD8⁺T 细胞介导的超敏反应中的治疗作用尚不明确。IV 型超敏反应(如接触性超敏反应、口腔苔藓样反应)由 CD8⁺T 细胞介导,现有治疗多以对症处理为主,缺乏靶向性。人脱落乳牙干细胞(Stem cells from human exfoliated deciduous teeth, SHED)作为 MSCs 亚型,具有优异的免疫调节能力,但其来源的凋亡囊泡(SHED-ApoVs)对免疫微环境及CD8⁺T 细胞的影响尚不明确。
近日,来自空军军医大学的研究团队通过构建小鼠接触性超敏反应(contact hypersensitivity, CHS)和口腔苔藓样反应(oral lichenoid reactions, OLR)两种模型,探究 SHED-ApoVs 对 CD8⁺T 细胞介导的 IV 型超敏反应的治疗作用及机制,并通过临床样本验证,为纳米囊泡基无细胞疗法提供理论依据。
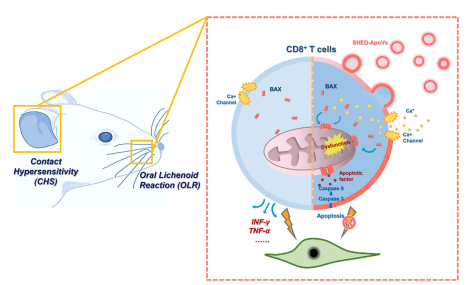
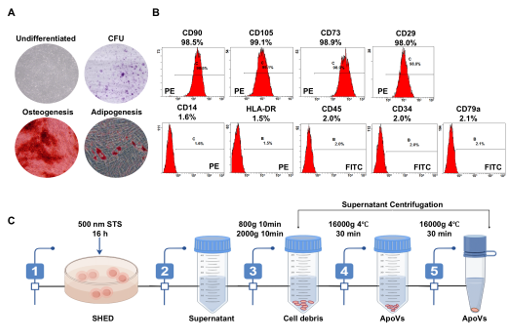
一、间充质干细胞及其来源的凋亡囊泡分离表征
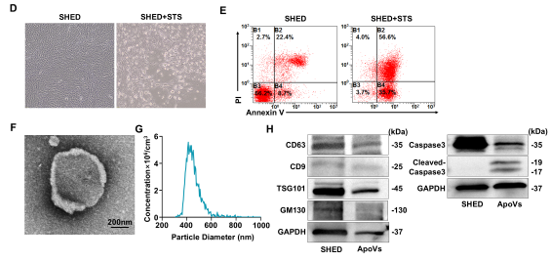
研究使用的人脱落乳牙干细胞SHED具有MSCs的一般特性,表达 MSCs 表面分子 CD90、CD105、CD73 和 CD29。采用星形孢菌素诱导凋亡,显微镜下可观察到 SHED 凋亡过程中的肿胀和球形化。透射电镜显示 ApoVs 呈典型的双膜球形结构。与未诱导的 SHED 相比,ApoVs 表达特异性凋亡相关标志物 cleaved-caspase3,表明从 SHED 分离的 ApoVs 具有高纯度的 MSCs 来源凋亡囊泡的特异性特征。
二、MSCs-ApoVs 减轻 CD8⁺T 细胞介导的接触性超敏反应
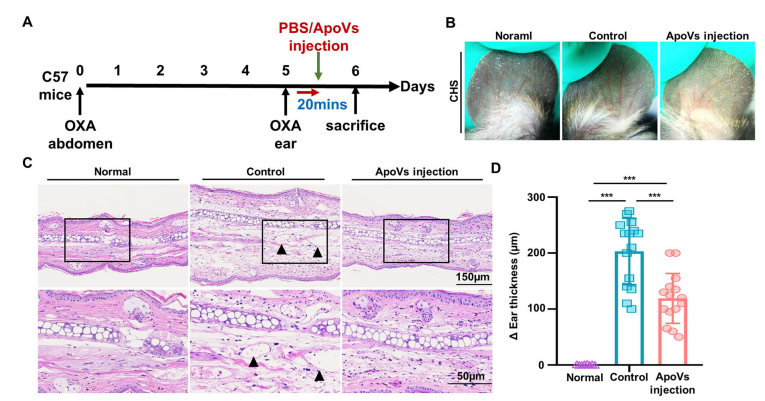
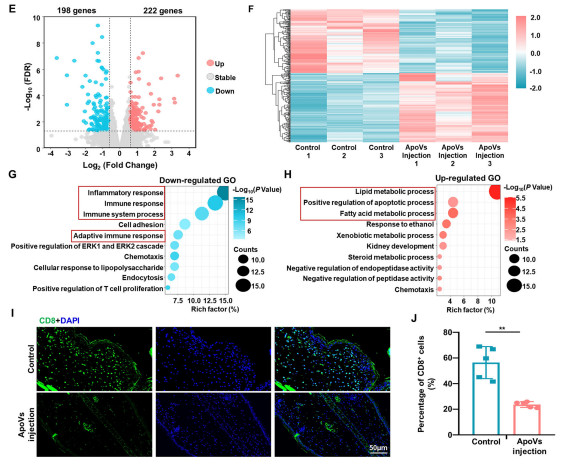
采用恶唑酮(OXA)作为半抗原构建小鼠接触性超敏反应模型,并注射 ApoVs。与正常组相比,对照组出现局部皮肤轻度充血和发红等激发反应,而 ApoVs 注射组反应减轻。对对照组和 ApoVs 注射组的耳样本进行 RNAseq,发现222 个上调和 198 个下调的差异表达基因。上调基因主要与代谢和凋亡过程相关,提示 ApoVs 处理可促进局部组织的代谢和凋亡过程,下调基因与炎症和免疫反应显著相关,提示耳部超敏反应导致组织炎症和免疫反应。ApoVs 处理后,免疫染色显示病变部位促炎 TNF-α⁺细胞表达减少,抗炎 TGF-β⁺细胞表达增加。ApoVs 注射 24 小时后,病变部位 CD8⁺T 细胞的比例降低。这些均表明SHED-ApoVs 处理可通过降低病变部位 CD8⁺T 细胞的比例,有效改善超敏反应诱导的炎症和免疫反应。
三、ApoVs 通过促进 CD8⁺T 细胞凋亡发挥抗超敏作用
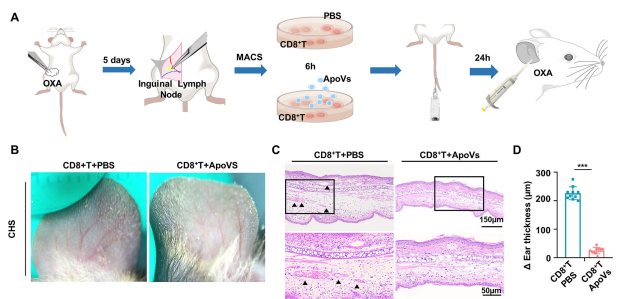
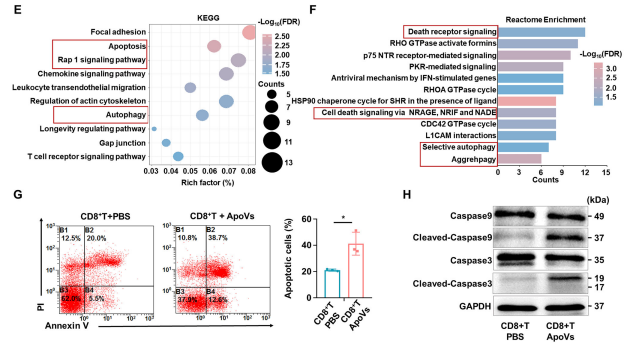
通过过继转移实验验证 ApoVs 是否在激发阶段通过特异性靶向 CD8⁺T 细胞减轻超敏反应。 ELISA 分析显示,ApoVs 处理后 CD8⁺T 细胞效应细胞因子(包括IFN-γ、TNF-α、穿孔素-1 和颗粒酶B)的表达降低。注射 ApoVs 处理的 CD8⁺T 细胞的受体小鼠耳部发红和肿胀显著低于注射PBS处理的 CD8⁺T 细胞的小鼠。研究观察到受体小鼠的耳部超敏反应依赖于注射的致敏CD8⁺T 细胞。这些发现表明,ApoVs 在超敏反应的激发阶段对 CD8⁺T 细胞具有直接抑制作用。以 PBS 处理的 CD8⁺T 细胞为对照,对 ApoVs 处理的 CD8⁺T 细胞进行 RNA seq,发现ApoVs 处理组的上调基因显著富集于凋亡相关信号通路。流式分析及细胞共定位发现ApoVs 处理显著诱导 CD8⁺T 细胞凋亡,表明 ApoVs 处理通过抑制 CD8⁺T 细胞功能并诱导其凋亡,显著改善超敏反应。
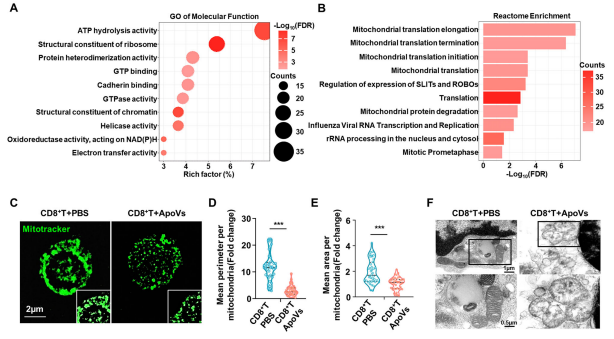
四、ApoVs 通过影响线粒体形态和功能诱导 CD8⁺T 细胞凋亡
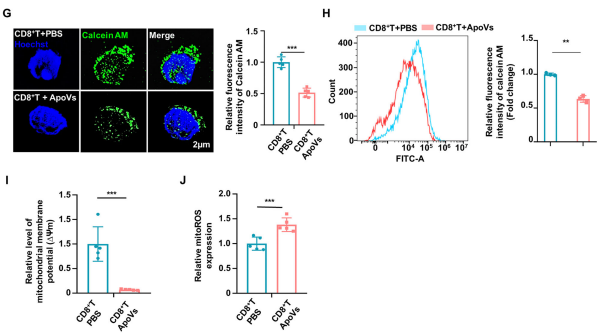
对ApoVs 进行蛋白质组学分析,发现上调蛋白质的前 10 个富集通路显著富集于线粒体功能相关,如 ATP 水解活性和电子传递活性,提示 ApoVs 通过影响线粒体通路诱导 CD8⁺T 细胞凋亡。追踪线粒体形态并进行线粒体膜电位检测后,发现ApoVs 处理导致 CD8⁺T 细胞的线粒体结构发生明显改变,表现为点状和碎片化形态,线粒体膜电位显著下降,表明ApoVs 处理通过影响线粒体的形态和功能诱导 CD8⁺T 细胞凋亡。
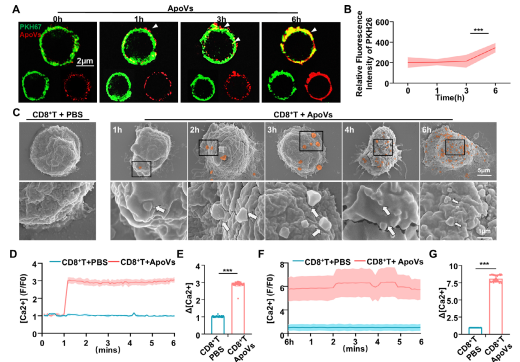
五、ApoVs 通过与 CD8⁺T 细胞膜融合引发钙内流
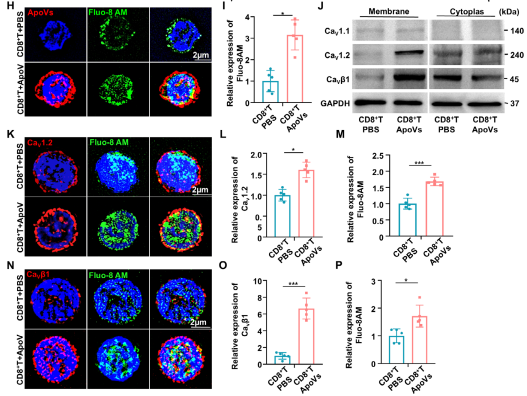
通过SIM² 荧光成像及扫描电镜观察到CD8⁺T 细胞膜上 ApoVs 的存在呈时间依赖性增加,ApoVs 处理 4 小时后观察到明显的膜融合,表明 SHED-ApoVs 主要通过膜融合诱导 CD8⁺T 细胞凋亡,导致线粒体功能障碍。Fluo-8AM 钙内流检测显示,ApoVs 处理可瞬时增加 CD8⁺T 细胞内钙离子水平,WB实验也发现ApoVs 处理可增强L 型钙通道蛋白 Cav1.2 和 Cavβ1 的膜表达,免疫荧光染色显示,ApoVs 处理后 CD8⁺T 细胞中 Cav1.2 和 Cavβ1 的表达水平随钙内流增加,表明ApoVs 通过与 CD8⁺T 细胞融合引发钙内流,导致L 型电压门控钙通道上调及随后的钙超载。
六、抑制 CD8⁺T 细胞钙内流可减弱 ApoVs 的疗效
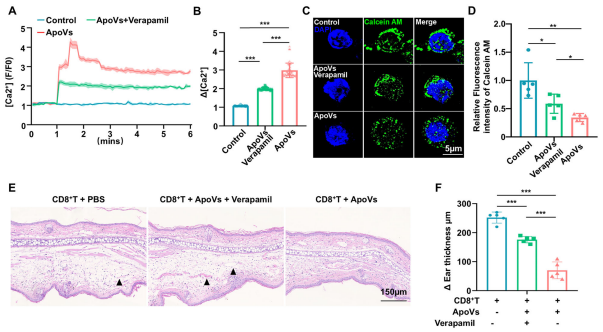
进一步用L 型钙通道抑制剂verapamil处理发现,抑制剂处理可减少 ApoVs 介导的细胞内钙内流,并减轻线粒体膜通透性,导致线粒体膜电位升高,线粒体 ROS 水平降低,表明抑制钙内流可改善线粒体功能。组织形态学观察和相对耳厚度测量进一步证实,阻断钙内流可降低 ApoVs 对接触性超敏反应小鼠的治疗效果。
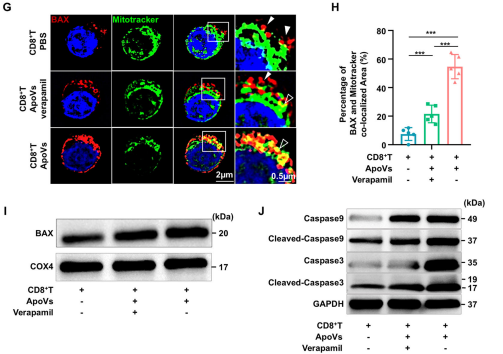
共定位染色和线粒体分离显示,ApoVs 处理后 CD8⁺T 细胞中 BAX(一种关键促凋亡蛋白) 与线粒体(Mitotracker)的共定位显著增加;使用verapamil抑制 L 型钙通道后,BAX 与 Mitotracker 的共定位显著减少。这些发现表明ApoVs 通过 L 型钙通道促进钙超载,诱导线粒体功能障碍,启动 CD8⁺T 细胞凋亡,从而改善 CHS 反应。
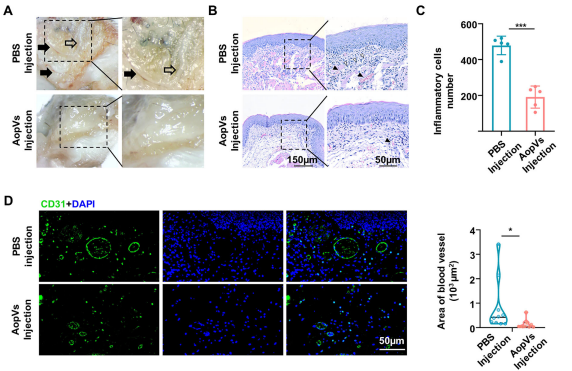
七、ApoVs 改善口腔苔藓样反应
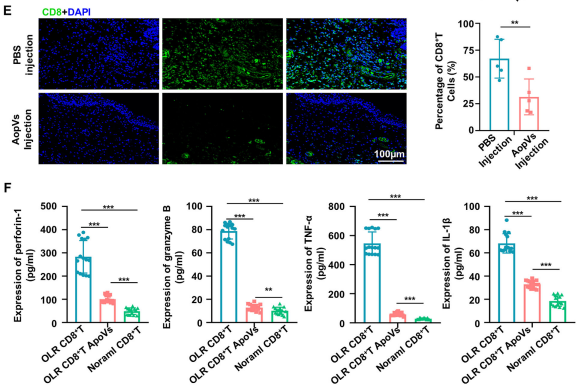
为进一步验证 ApoVs 在 IV 型超敏反应中的治疗效果,构建了另一种口腔苔藓样 OLR 小鼠模型(病理上属于 IV 型超敏反应)。激发阶段,在小鼠颊黏膜涂抹 OXA 后可观察到网状条纹,H&E染色可见黏膜下层带状淋巴细胞浸润,与口腔扁平苔藓(OLP)特征高度相似ApoVs 注射处理组中,这些炎症表现显著减轻。免疫染色显示,与 PBS 注射相比,ApoVs 注射可减轻血管重塑,降低 TNF-α 表达。且注射后 CD8⁺T 细胞的比例也降低。收集 3 名健康志愿者和 3 名 OLR 患者的外周血样本,富集并激活 CD8⁺T 细胞,用 ApoVs 或 PBS 处理 OLR 患者的 CD8⁺T 细胞,发现体外 ApoVs 处理可显著降低患者 CD8⁺T 细胞分泌的穿孔素-1、颗粒酶B、TNF-α 和IL-1β水平。此外,ApoVs 处理后,患者 CD8⁺T 细胞线粒体通透性增加,与 CHS 模型结果一致。文章数据表明,MSCs来源的 ApoVs 可诱导 CD8⁺T 细胞凋亡,改善 CD8⁺T 细胞介导的 IV 型超敏反应,为 MSCs 来源 ApoVs 的临床前和临床研究提供了新见解。
吉凯现有转录组+蛋白组联合的优惠活动,下周二还有转录+蛋白联合的直播课,感兴趣的小伙伴们欢迎扫码咨询哦👇👇👇