上海吉凯基因医学科技股份有限公司品牌商
15 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
公司新闻/正文
免疫肽组——连接机体蛋白状态与免疫应答的桥梁
398 人阅读发布时间:2025-09-18 09:54

免疫肽通常指能够被免疫系统识别并与免疫细胞上的特定受体结合的肽段,这些肽段主要来源于两大途径——内源性途径:机体自身细胞的蛋白质(包括正常蛋白、突变蛋白、病毒/细菌等病原体入侵后产生的外源蛋白)经蛋白酶体降解,生成的多肽被转运至细胞表面,与主要组织相容性复合体(major histocompatibility complex, MHC,人类中主要是人白细胞抗原human leukocyte antigen, HLA)结合,形成 “MHC-肽复合物”;外源性途径:免疫细胞(如树突状细胞、巨噬细胞)吞噬外源病原体或凋亡细胞后,其内部蛋白质被溶酶体降解为多肽,再与 MHC分子结合并呈递到细胞表面。
免疫肽组(immunopeptidome)是对有核细胞在参与抗原呈递途径中的MHC抗原上呈递的全部多肽进行研究,通过免疫沉淀和质谱技术鉴定不同的免疫肽(主要是MHC I类或II类),对于探究细胞介导和体液反应介导中的免疫原性表位至关重要。
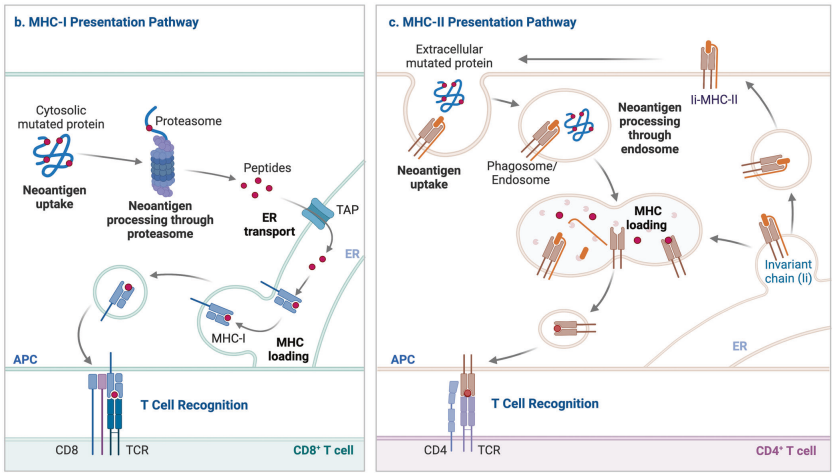
MHC-I和MHC-II呈递肿瘤抗原的途径[1]
免疫肽组通过免疫沉淀特异性地富集目标蛋白或多肽,可减少样本中其他成分的干扰,提高后续质谱分析的准确性和可靠性,同时,通过质谱直接分析肿瘤细胞表面的肽段,能够高通量地鉴定和定量复杂多肽样品中的组分,得到更精确的抗原肽的信息,从而揭示肿瘤特异性抗原。作为连接机体蛋白状态与免疫应答的桥梁,免疫肽组在疾病诊疗、药物开发等领域具有不可替代的应用潜力。
免疫肽组技术路线
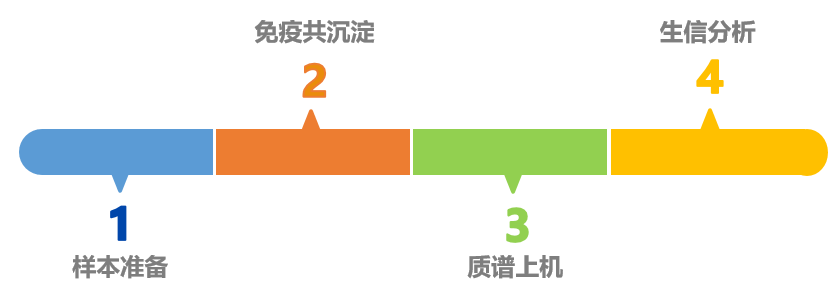
样本准备
样本选择(组织/细胞等)
蛋白提取(含蛋白酶抑制剂裂解液,超声/冰上孵育)
免疫共沉淀
磁珠结合抗体孵育(用IgG去除非特异结合)
抗体捕获、免疫沉淀(抗体与磁珠结合,室温孵育或4℃过夜)
磁珠洗涤(多次清洗)
质谱上机
质谱前处理(脱盐、浓缩等)
LC-MS/MS检测(肽段分离与鉴定)
质谱数据库检索(匹配蛋白数据库)
生信分析
MHC亲和力预测、TCR免疫原性预测
免疫多肽表达差异分析、蛋白来源分析
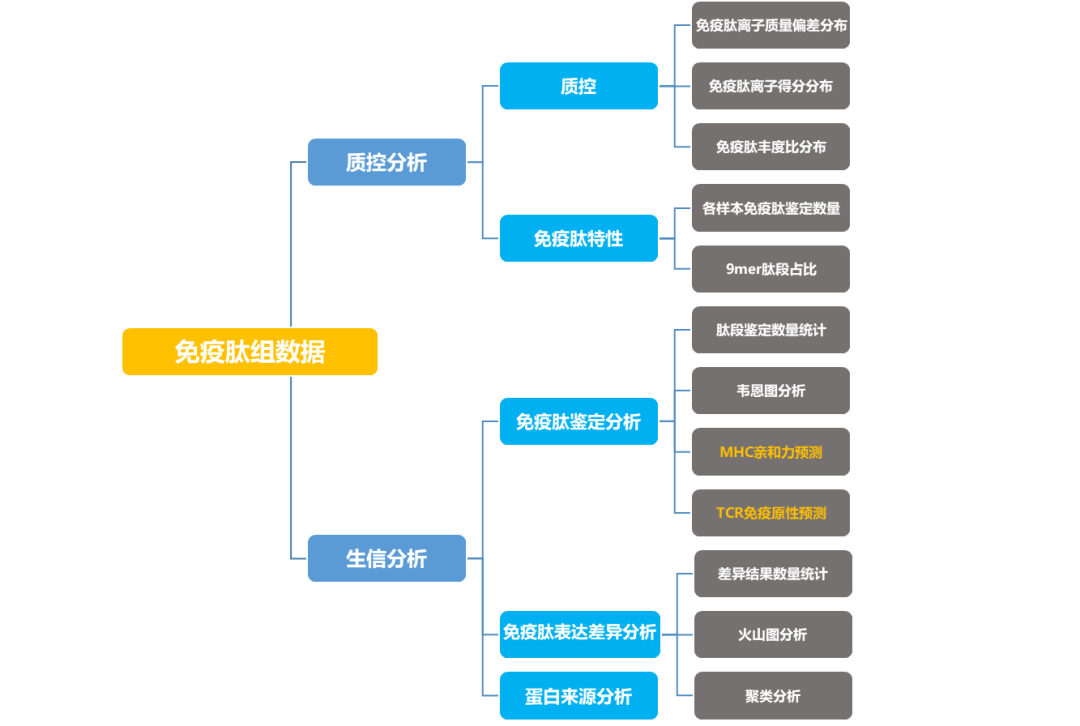
免疫肽组数据分析流程
免疫肽组应用案例

研究背景
XPO1 (Exportin-1/CRM1)是一种核输出蛋白,在癌症中经常过表达,并作为肿瘤发生的驱动因素。目前,靶向XPO1的小分子正被用作临床抗癌药物。自然杀伤(NK)细胞在抗肿瘤免疫中作用日益凸显,其功能受多种细胞表面受体精密调控,杀伤细胞免疫球蛋白样受体(KIRs)是其中关键家族。KIR分为激活型和抑制型,抑制型 KIR 的人类白细胞抗原HLA I类配体特异性已较明确,但激活型 KIR 的配体特异性难以鉴定。激活型KIR2DS2与血液系统恶性肿瘤复发保护、多种实体瘤(如肝细胞癌、乳腺癌等)防护相关,但缺乏功能相关性验证。
研究目的
探究是否存在由肿瘤相关蛋白衍生的、可被激活型 KIR2DS2 识别的肽配体,验证核输出蛋白XPO1是否为KIR2DS2的靶标,及其衍生肽与KIR2DS2、HLA-C的互作机制。
样本信息
细胞样本(肝癌细胞/淋巴细胞/NK细胞)及患者样本(KIR2DS2 阳性肝细胞癌患者的PBMC)
组学策略
免疫肽组+转录组(TCGA数据库)
主要结论
XPO1 是自然杀伤(NK)细胞的作用靶点。通过免疫肽组学技术鉴定出一种源自XPO1的肽段,该肽段在人类白细胞抗原-C(HLA-C)的作用背景下,可被 NK 细胞的激活型受体 KIR2DS2 识别。这种肽段能够在细胞内被加工呈递,并通过该受体特异性激活 NK 细胞。尽管癌症中 XPO1 的高表达通常与不良预后相关,但本文研究表明,对于肝细胞癌等特定癌症,若同时存在 NK 细胞浸润的证据,患者的预后可得到显著改善。研究证实 XPO1 是 NK 细胞识别的真实肿瘤抗原,其高表达联合 NK 细胞浸润可作为癌症预后分层标志,基于肽-HLA的靶向策略或CAR-NK 细胞疗法有望实现实体瘤的个性化NK细胞治疗[2]。
吉凯现可开展免疫肽组技术服务,通过MHC抗体特异性富集结合高分辨质谱检测,可检测到ng/ml级别的物质,并直接提供免疫肽序列,协助您发现与特定疾病相关的微量多肽并筛选出可靠新抗原,为您在肿瘤诊疗与分型、疾病诊断与疫苗研发、免疫性疾病发病机制与治疗等方向提供新的思路及策略。9月25日还有免疫肽组相关的直播讲座,感兴趣的小伙伴们欢迎扫码关注哦!

【参考文献】
1.Xie Na., et al. Neoantigens: promising targets for cancer therapy. Signal Transduct Target Ther.2023.
2.Matthew D Blunt., et al. The nuclear export protein XPO1 provides a peptide ligand for natural killer cells. Sci Adv. 2024.